
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ,密度之比为 .
(2)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是 ,含原子数最多的是 ,体积最小的是 .
考点:
物质的量的相关计算.
专题:
计算题.
分析:
(1)同温同压下,气体的Vm相等,n=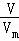 =
=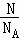 结合分子的构成以及ρ=
结合分子的构成以及ρ=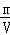 =
=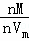 =
=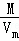 计算;
计算;
(2)根据n=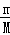 =
=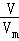 =
=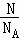 计算.
计算.
解答:
解:(1)同温同压下,气体的Vm相等,由n=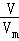 =
=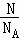 可知,同体积的甲烷(CH4)和二氧化碳分子数之比为1:1,物质的量之比为1:1,原子总数之比为5:3,
可知,同体积的甲烷(CH4)和二氧化碳分子数之比为1:1,物质的量之比为1:1,原子总数之比为5:3,
由ρ=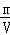 =
=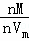 =
=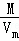 可知,密度之比为两种气体的摩尔质量之比,为16:44=4:11,
可知,密度之比为两种气体的摩尔质量之比,为16:44=4:11,
故答案为:1:1;1:1;5:3;4:11;
(2)n(H2)=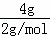 =2mol,n(O2)=
=2mol,n(O2)=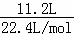 =0.5mol,n(H2O)=1mol,
=0.5mol,n(H2O)=1mol,
由n=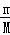 =
=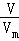 =
=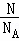 可知,分子数最多的是H2,原子数最多的是H2,标准状况下水为液体,体积最小,
可知,分子数最多的是H2,原子数最多的是H2,标准状况下水为液体,体积最小,
故答案为:H2;H2;H2O.
点评:
本题考查物质的量的相关计算,侧重于学生的分析能力和计算能力的考查,为高频考点,注意把握相关计算公式以及物质存在的体积和状态,为解答该题的易错点,难度中等.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
下列有关实验的叙述正确的是( )
-A.-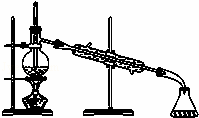
实验室蒸馏石油
-B.-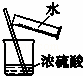
实验室稀释浓硫酸
-C.-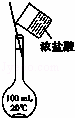
配制100 mL 0.1 mol•L﹣1 的盐酸
-D.-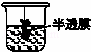
可用于分离或提纯胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ,密度之比为 .
(2)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是 ,含原子数最多的是 ,体积最小的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,Na+浓度最大的是( )
|
| A. | 5L 1.2mol•L﹣1的Na2SO4溶液 |
|
| B. | 2L 0.8mol•L﹣1的NaOH溶液 |
|
| C. | 1L 1mol•L﹣1的Na2CO3溶液 |
|
| D. | 4L 0.5mol•L﹣1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 1molCH3+(碳正离子)含有9 NA个电子 |
|
| B. | 2.5molHe 中含有10 NA个质子 |
|
| C. | 6.02×1022 个H2SO4分子在溶液中可电离出2NA个H+ |
|
| D. | 1molFe与盐酸完全反应可失去电子的物质的量为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
在给定的四种溶液中加入以下各种离子,各离子能在原溶液中共存的是()
A. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl﹣、SCN﹣
B. pH为1的溶液:Cu2+、Na+、Mg2+、NO3﹣
C. 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+
D. 所含溶质为Na2SO4的溶液:K+、CO32﹣、NO3﹣、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列热化学方程式:
Zn(s)+O2(g)═ZnO(s)△H=﹣Q1 kJ/mol
Hg(l)+O2(g)═HgO(s)△H=﹣Q2kJ/mol
Zn(s)+HgO(s)═Hg(l)+ZnO(s)△H=﹣Q3kJ/mol
Q3值为()
A. Q2﹣Q1 B. Q1+Q2 C. Q1﹣Q2 D. ﹣Q1﹣Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知N≡N、N﹣H、H﹣H的键能分别为946kJ•mol﹣1、390.8kJ•mol﹣1、436.0kJ•mol﹣1.试根据盖斯定律,写出合成氨反应的热化学方程式 .
(2)在通常状况下,足量氢氧化钠的稀溶液与含溶质为1mol的稀硫酸完全反应时放出akJ的热量,写出该反应中和热的热化学方程式
(3)以镁和铝为电极,以NaOH作电解质溶液,构成原电池时,铝做负极,电极反应式为 ;
与MnO2﹣Zn电池类似,K2FeO4﹣Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为 ,该电池总反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ•mol﹣1)P﹣P:198 P﹣O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为()

A. +1638KJ•mol﹣1 B. ﹣1638KJ•mol﹣1
C. +126KJ•mol﹣1 D. ﹣126KJ•mol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com