
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A.±ź×¼×“æöĻĀ£¬22.4LĖ®µÄ·Ö×ÓŹżÄæĪŖNA
B.±ź×¼×“æöĻĀ£¬11.2Lŗ¤Ęųŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖNA
C.³£ĪĀ³£Ń¹ĻĀ£¬48 g O3ŗ¬ÓŠµÄŃõŌ×ÓŹżÄæĪŖ3NA
D.0.5 mol”¤L£1µÄMgCl2ČÜŅŗÖŠ£¬ŗ¬ÓŠCl£µÄŹżÄæĪŖNA
”¾“š°ø”æC
”¾½āĪö”æ
A. ±ź×¼×“æöĻĀ£¬Ė®ŹĒŅŗĢ壬²»ÄÜÓĆĘųĢåĦ¶ūĢå»ż½ųŠŠ¼ĘĖć£¬¹ŹA“ķĪó£»
B. ±ź×¼×“æöĻĀ£¬11.2Lŗ¤ĘųĪļÖŹµÄĮæ![]() £¬ÓÉÓŚŗ¤ĘųŹĒµ„Ō×Ó·Ö×Ó£¬Ņņ“Ė11.2Lŗ¤Ęųŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖ0.5NA£¬¹ŹB“ķĪó£»
£¬ÓÉÓŚŗ¤ĘųŹĒµ„Ō×Ó·Ö×Ó£¬Ņņ“Ė11.2Lŗ¤Ęųŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖ0.5NA£¬¹ŹB“ķĪó£»
C. ³£ĪĀ³£Ń¹ĻĀ£¬48 g O3ĪļÖŹµÄĮæ![]() £¬Ņņ“ĖÓŠµÄŃõŌ×ÓŹżÄæĪŖ3NA£¬¹ŹCÕżČ·£»
£¬Ņņ“ĖÓŠµÄŃõŌ×ÓŹżÄæĪŖ3NA£¬¹ŹCÕżČ·£»
D. 0.5 mol”¤L£1µÄMgCl2ČÜŅŗÖŠ£¬Č±ÉŁČÜŅŗĢå»ż£¬ĪŽ·Ø¼ĘĖć£¬¹ŹD“ķĪó”£
×ŪÉĻĖłŹö£¬“š°øĪŖC”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²Ł×÷ÓėŌ¤ĘŚŹµŃéÄæµÄ»ņĖłµĆŹµŃé½įĀŪŅ»ÖĀµÄŹĒ
Ń”Ļī | ŹµŃé²Ł×÷ŗĶĻÖĻó | Ō¤ĘŚŹµŃéÄæµÄ»ņ½įĀŪ |
A | ÓĆ½ą¾»µÄ²¬ĖæÕŗČ”Ä³Ź³ŃĪŹŌŃł£¬ŌŚ¾Ę¾«µĘ»šŃęÉĻ×ĘÉÕ£¬»šŃęĻŌ»ĘÉ« | ĖµĆ÷øĆŹ³ŃĪŹŌŃł²»ŗ¬KIO3 |
B | SiO2ÄÜÓėĒā·śĖį¼°¼ī·“Ó¦ | SiO2ŹĒĮ½ŠŌŃõ»ÆĪļ |
C | ĻņĮ½Ö§Ź¢ÓŠKI3µÄČÜŅŗµÄŹŌ¹ÜÖŠ£¬·Ö±šµĪ¼Óµķ·ŪČÜŅŗŗĶAgNO3ČÜŅŗ£¬Ē°ÕßČÜŅŗ±äĄ¶£¬ŗóÕßÓŠ»ĘÉ«³Įµķ | KI3ČÜŅŗÖŠ“ęŌŚĘ½ŗā£ŗ |
D | ŹŅĪĀĻĀĻņCuCl2ŗĶÉŁĮæFeCl3µÄ»ģŗĻČÜŅŗÖŠ£¬¼ÓČėĶŠ¼£¬³ä·Ö½Į°č£¬¹żĀĖ£¬µĆĄ¶ĀĢÉ«ČÜŅŗ | ³żČ„ŌÓÖŹFeCl3µĆ“æ¾»CuCl2ČÜŅŗ |
A.AB.BC.CD.D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ¢ŁH2(g)+ ![]() O2(g)=H2O(g)£»¦¤H1= akJ”¤mol-1
O2(g)=H2O(g)£»¦¤H1= akJ”¤mol-1
¢Ś2H2(g)+O2(g) = 2H2O(g)£»¦¤H2= b kJ”¤mol-1 ¢Ū H2(g)+ ![]() O2(g)=H2O(l)£»¦¤H3= c kJ”¤mol-1
O2(g)=H2O(l)£»¦¤H3= c kJ”¤mol-1
¢Ü2H2(g)+O2(g) = 2H2O(l)£»¦¤H4= d kJ”¤mol-1£¬ĻĀĮŠ¹ŲĻµŹ½ÖŠÕżČ·µÄŹĒ( )
A.2a=b<0B.b>d>0C.a<c<0D.2c=d>0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°¢ĪŗĖįŌŚŹ³Ę·”¢Ņ½Ņ©µČ·½Ćęӊ׏ć·ŗÓĆĶ¾”£Ņ»ÖÖŗĻ³É°¢ĪŗĖįµÄ·“Ó¦æɱķŹ¾ĪŖ£ŗ
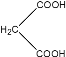
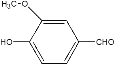 +
+
![]()
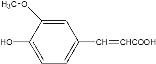 +H2O+CO2
+H2O+CO2
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A.æÉÓĆĖįŠŌ![]() ČÜŅŗ¼ģ²āÉĻŹö·“Ó¦ŹĒ·ńÓŠ°¢ĪŗĖįÉś³É
ČÜŅŗ¼ģ²āÉĻŹö·“Ó¦ŹĒ·ńÓŠ°¢ĪŗĖįÉś³É
B.ĻćĄ¼ĖŲ”¢°¢ĪŗĖį¾łæÉÓė![]() ”¢
”¢![]() ČÜŅŗ·“Ó¦
ČÜŅŗ·“Ó¦
C.Ķس£Ģõ¼žĻĀ£¬ĻćĄ¼ĖŲ.°¢ĪŗĖį¶¼ÄÜ·¢ÉśČ”“ś”¢¼Ó³É”¢Ńõ»Æ·“Ó¦
D.![]() ĻćĄ¼ĖŲ×ī¶ąæÉŅŌÓė
ĻćĄ¼ĖŲ×ī¶ąæÉŅŌÓė![]() ·¢Éś¼Ó³É·“Ó¦
·¢Éś¼Ó³É·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖHAµÄĖįŠŌĒæÓŚHBµÄĖįŠŌ”£25”ꏱ£¬ÓĆNaOH¹ĢĢå·Ö±šøıäĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.1 molL-1µÄHAČÜŅŗŗĶHBČÜŅŗµÄpH(ČÜŅŗµÄĢå»ż±ä»ÆŗöĀŌ²»¼Ę)£¬ČÜŅŗÖŠA-”¢B-µÄĪļÖŹµÄĮæÅØ¶ČµÄøŗ¶ŌŹżÓėČÜŅŗµÄpHµÄ±ä»ÆĒéæöČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
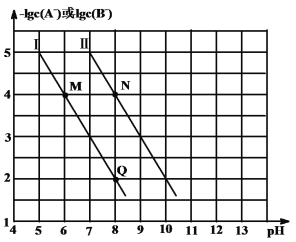
A.ĒśĻߢń±ķŹ¾ČÜŅŗµÄpHÓė-lgc(B-)µÄ±ä»Æ¹ŲĻµ
B.Ka(HA)”ĆKa(HB)=1000”Ć1
C.ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č£ŗM<N
D.Nµć¶ŌÓ¦µÄČÜŅŗÖŠc(Na+)£¾Qµć¶ŌÓ¦µÄČÜŅŗÖŠc(Na+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ
ø£·ÓĆĄæĖŹĒŅ»ÖÖÓ°Ļģ»śĢåĆāŅßĮ¦¹¦ÄܵÄŅ©Īļ£¬æÉĶعżŅŌĻĀ·½·ØŗĻ³É£ŗ
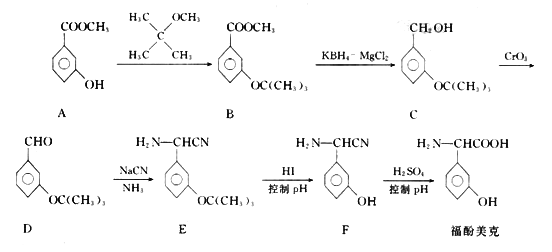
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ĪļÖŹAµÄŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖ___________£»B”śCµÄ×Ŗ»ÆŹōÓŚ___________·“Ó¦(Ģī·“Ó¦ĄąŠĶ)
(2)ÉĻŹöĮ÷³ĢÖŠÉč¼ĘA”śB²½ÖčµÄÄæµÄŹĒ________£»F·Ö×ÓÖŠ¹²Ę½ĆęµÄŌ×Ó×ī¶ąÓŠ________øö”£
(3)DÓėŅų°±ČÜŅŗ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________”£
(4)ø£·ÓĆĄæĖ¾ßÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壮Š“³öĘäÖŠ·ūŗĻĻĀĮŠĢõ¼žµÄÓŠ»śĪļ½į¹¹¼ņŹ½£ŗ___________ŗĶ___________”£
¢Łŗ¬ÓŠ£CONH2£»
¢ŚÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£»
¢ŪŗĖ“Ź²ÕńĒāĘ×µÄĪüŹÕ·åŹżÄæÓŠ4øö”£
(5)²ĪÕÕÉĻŹöŗĻ³ÉĀ·ĻßŗĶŠÅĻ¢£¬ŅŌŅŅ“¼ĪŖŌĮĻ(ĪŽ»śŹŌ¼ĮČĪŃ”)£¬Éč¼ĘÖĘ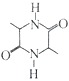 µÄŗĻ³ÉĀ·Ļߣŗ___________”£
µÄŗĻ³ÉĀ·Ļߣŗ___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŠĀŅ©HµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĶ¼£ŗ
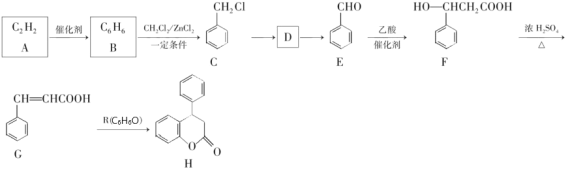
ŅŃÖŖ£ŗAÄÜŹ¹äåĖ®ĶŹÉ«£¬RÓöĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦”£
(1)RµÄĆū³ĘŹĒ____________________£»GÖŠĖłŗ¬¹ŁÄÜĶÅĆū³ĘŹĒ______________”£
(2)C”śDµÄ·“Ó¦Ģõ¼žŗĶŹŌ¼ĮŹĒ____________£»E”śFµÄ·“Ó¦ĄąŠĶŹĒ___________”£
(3)ÄܼģŃéHŗ¬õ„»łµÄŅĒĘ÷Ćū³ĘŹĒ_________”£A”śBµÄŌ×ÓĄūÓĆĀŹĪŖ___________”£
(4)Š“³öD”śEµÄ»Æѧ·½³ĢŹ½£ŗ____________”£
(5)ŌŚGµÄĶ¬·ÖŅģ¹¹ĢåÖŠ£¬Ķ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ_______ÖÖ”£
¢ŁŹōÓŚ±½µÄŃÜÉśĪļ£»
¢ŚÄÜ·¢ÉśĖ®½ā·“Ó¦ŗĶŅų¾µ·“Ó¦£»
¢ŪÄÜÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ·¢Éś¼Ó³É·“Ó¦”£
(6)²ĪÕÕÉĻŹöŗĻ³ÉĀ·Ļߣ¬Éč¼ĘŅ»ĢõÓÉŅŅĻ©”¢ŅŅĖįĪŖŌĮĻÖʱø![]() µÄŗĻ³ÉĀ·Ļß__________
µÄŗĻ³ÉĀ·Ļß__________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŗćĪĀŗćČŻµÄĆܱÕČŻĘ÷ÖŠĶØČėlmolXŗĶ2molY£¬·¢ÉśĻĀĮŠ·“Ó¦:X(g)+2Y(g)![]() M(g)+2N(g) ”÷H=akJ/mol(a>0)£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
M(g)+2N(g) ”÷H=akJ/mol(a>0)£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A. µ½“ļĘ½ŗāדĢ¬Ź±£¬¼ÓČė“߻ƼĮ£¬Ę½ŗā²»ŅĘ¶Æ£¬·“Ó¦ĖŁĀŹŅ²²»»į·¢Éśøıä
B. ·“Ó¦“ļµ½Ę½ŗāŹ±£¬XŗĶYµÄ×Ŗ»ÆĀŹĻąµČ
C. vÕż(X)=2vÄę(N)Ź±£¬·“Ó¦µ½“ļĘ½ŗāדĢ¬
D. µ½“ļĘ½ŗāדĢ¬Ź±£¬·“Ó¦ĪüŹÕakJÄÜĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ÖÖŅŌ»ŌĶæó(Ö÷ŅŖ³É·ÖĪŖCu2S£¬ŗ¬ÉŁĮæSiO2£©ĪŖŌĮĻÖʱøĻõĖįĶµÄ¹¤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ

£Ø1£©Š“³ö”°½žČ””±¹ż³ĢÖŠCu2SČܽāŹ±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ___”£
£Ø2£©ŗćĪĀ”°½žČ””±µÄ¹ż³ĢÖŠ·¢ĻÖĶŌŖĖŲµÄ½žČ”ĖŁĀŹĻČŌö“óŗó¼õÉŁ£¬ÓŠŃŠ¾æÖø³öCuCl2ŹĒøĆ·“Ó¦µÄ“߻ƼĮ£¬øĆ¹ż³ĢµÄ·“Ó¦ŌĄķæÉÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ£ŗ¢ŁCu2S +2CuCl2=4CuCl+S£»¢Ś___”£
£Ø3£©”°»ŲŹÕS”±¹ż³ĢÖŠĪĀ¶ČæŲÖĘŌŚ50”«60”ęÖ®¼ä£¬²»ŅĖ¹żøßµÄŌŅņŹĒ___”£
£Ø4£©ĻņĀĖŅŗMÖŠ¼ÓČė(»ņĶØČė)___(Ģī×ÖÄø)£¬æɵƵ½Ņ»ÖÖæÉŃ»·ĄūÓƵÄĪļÖŹ”£
a.Ģś b.ĀČĘų c.øßĆĢĖį¼Ų d.ĀČ»ÆĒā
£Ø5£©”°±£ĪĀ³żĢś”±¹ż³ĢÖŠ£¬¼ÓČėCuOµÄÄæµÄŹĒ__£»”°Õō·¢ÅØĖõ”¢ĄäČ“½į¾§”±¹ż³ĢÖŠ£¬ŅŖÓĆHNO3ČÜŅŗµ÷½ŚČÜŅŗµÄpH£¬ĘäĄķÓÉ_”£
£Ø6£©»ŌĶæóæÉÓÉ»ĘĶæó(Ö÷ŅŖ³É·ÖĪŖCuFeS2)Ķعżµē»Æѧ·“Ó¦×Ŗ±ä¶ų³É£¬ÓŠ¹Ų×Ŗ»Æ¼ūĶ¼£¬×Ŗ»ÆŹ±×ŖŅĘ0.2molµē×Ó£¬Éś³ÉCu2S___mol”£

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com