
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
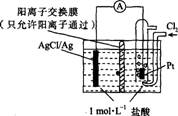
A.正极反应为AgCl+e-═Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
【答案】D
【解析】
试题分析:根据电池总反应为2Ag+Cl2═2AgCl可知,Ag失电子作负极失电子,氯气在正极上得电子生成氯离子,则A、正极上氯气得电子生成氯离子,其电极反应为:Cl2+2e-═2Cl-,故A错误;B、放电时,交换膜左侧溶液中生成银离子,银离子与氯离子反应生成氯化银沉淀,所以交换膜左侧溶液中有大量白色沉淀生成,故B错误;C、根据电池总反应为2Ag+Cl2═2AgCl可知,用NaCl溶液代替盐酸,电池的总反应不变,故C错误;D、放电时,当电路中转移0.01mol e-时,交换膜左则会有0.01mol氢离子通过阳离子交换膜向正极移动,同时会有0.01molAg失去0.01mol电子生成银离子,银离子会与氯离子反应生成氯化银沉淀,所以氯离子会减少0.01mol,则交换膜左侧溶液中约减少0.02mol离子,故D正确,故选:D。
考点:考查原电池原理的应用及沉淀反应


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.硫酸和磷酸的摩尔质量不相等
B.18 g水中含有1 mol水
C.O2的摩尔质量(单位是g·mol-1)在数值上等于其相对分子质量
D.1 mol CO的质量是28 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于加成反应的是
A.CH4+Cl2  CH3Cl+HCl
CH3Cl+HCl
B.CH2=CH2 + HCl 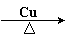 CH3CH2Cl
CH3CH2Cl
C.2CH3 CH2OH + O2 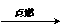 2CH3 CHO+2H2O
2CH3 CHO+2H2O
D.2C6H6 + 15O2 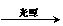 12CO2 +6H2O
12CO2 +6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A.HF稳定性比HCl强 B.Mg失电子能力比Ca弱
C.NaCl与NH4Cl含有的化学键类型相同 D.等物质的量的C2H6和H2O2含电子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是
A.由H+(aq)+OH-(aq)=H20(1) △H=-57.3 kJ·mol-1,可知含1 mo1 CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量为57.3 kJ
B.由C(石墨)=C(金刚石) △H=+1.9 kJ·mol-1,可知石墨比金刚石更稳定
C.由N2(g)+3H2(g)=2NH3(g) △H=-92.4 kJ·mol-1,可知将1 mol N2(g)和3 mol H2(g)置于密闭容器中充分反应后放出热量为92.4 kJ
D.由△G=△H-T△S可知,所有的放热反应都能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年10月24日双鸭山市区发生严重的雾霾天气,对人们的健康造成严重威胁,环境问题离我们也并不遥远了,则下列有关环境问题说法正确的是( )
A. PH<7的雨水称为酸雨
B. 二氧化硫的大量排放是造成光化学烟雾的主要原因
C. PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生相关
D. SO2、CO2、NO2均属于大气污染物
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、NH4+、Cl﹣、SO42﹣、NO3﹣中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )

|
| A. | 一定没有Cu2+、NO3﹣、Cl﹣ | B. | 可能有K+、NH4+、NO3﹣、SO42﹣ |
|
| C. | 不能确定是否含有K+、NO3﹣ | D. | 一定有Mg2+、Al3+、Cl﹣、SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸(H2C2O4)是二元中强酸,酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.
Ⅰ、某探究小组利用该反应,用浓度为0.1000mol•L﹣1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的离子方程式为 2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O .
(2)滴定过程中操作滴定管的图示正确的是 A .
(3)本滴定达到终点的标志是: 当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点
(4)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度 偏高 ,
(填“偏高”、“偏低”、或“不变”).
Ⅱ、草酸氢钠溶液显酸性,常温下,向10mL 0.01mol/LNaHC2O4溶液中滴加0.01mol/LNaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是: BD
A、V(NaOH)=0时,c(H+)=1×10﹣2 mol/L
B、V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42﹣)+c(HC2O4﹣)
C、V(NaOH)=10mL时,c(H+)=1×10﹣7 mol/L
D、V(NaOH)>10mL时,c(Na+)>c(C2O42﹣)>c(HC2O4﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
往含Fe3+、H+、NO3﹣的混合液中加入少量含SO32﹣的某溶液充分反应后(设溶液中的其他成分不反应),下列表示该混合溶液中发生反应的离子方程式中正确的是( )
|
| A. | 2 Fe3++SO32﹣+H2O→2 Fe2++SO42﹣+2 H+ |
|
| B. | 2 H++SO32﹣→SO2↑+H2O |
|
| C. | 2 H++2 NO3﹣+3 SO32﹣→3 SO42﹣+2 NO+H2O |
|
| D. | 2 Fe3++3 SO32﹣+3 H2O→2 Fe(OH)3↓+3 SO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com