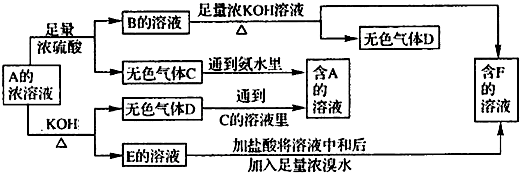
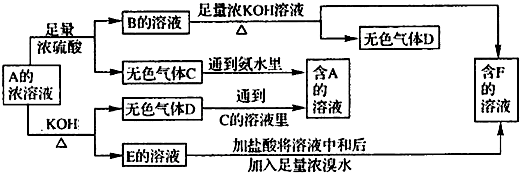
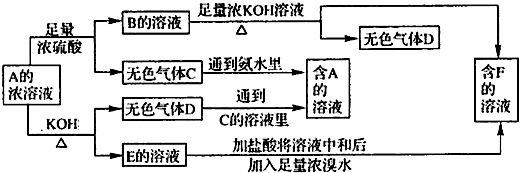
解:(1)由C+氨水→A,D+C的溶液→A,知D为NH
3,则A为铵盐,由A可跟酸反应,又可与碱反应且A为正盐且为弱酸弱碱盐,A与浓硫酸反应生成B是(NH
4)
2SO
4,推知F为K
2SO
4,E为K
2SO
3,C为SO
2,即A为(NH
4)
2SO
3,B为(NH
4)
2SO
4,C为SO
2,D为NH
3,E为K
2SO
3,F为K
2SO
4,故答案为:(NH
4)
2SO
3;SO
2;NH
3;
(2)A→D为(NH
4)
2SO
3 和KOH的反应,反应的离子方程式为NH
4++OH
-
NH
3↑+H
2O,
故答案为:NH
4++OH
-
NH
3↑+H
2O;
(3)SO
32-具有还原性,与具有氧化性的Br
2发生氧化还原反应生成SO
42-和Br
-,
反应的离子方程式为SO
32-+Br
2+H
2O=SO
42-+2Br
-+2H
+,
故答案为:SO
32-+Br
2+H
2O=SO
42-+2Br
-+2H
+;
(4)可分别检验K
+和SO
42-,可用焰色反应鉴定K
+,隔蓝色钴玻璃,火焰呈紫色,用BaCl
2检验SO
42-,具体做法为通过焰色反应鉴定K
+(隔蓝色钴玻璃,火焰呈紫色);取少量F的溶液加入BaCl
2和盐酸的溶液,若产生白色沉淀,证明SO
42-的存在,
故答案为:通过焰色反应鉴定K
+(隔蓝色钴玻璃,火焰呈紫色);取少量F的溶液加入BaCl
2和盐酸的溶液,若产生白色沉淀,证明SO
42-的存在.
分析:由C+氨水→A,D+C的溶液→A,知D为NH
3,则A为铵盐,由A可跟酸反应,又可与碱反应且A为正盐且为弱酸弱碱盐,A与浓硫酸反应生成B是(NH
4)
2SO
4,推知F为K
2SO
4,E为K
2SO
3,
C为SO
2,即A为(NH
4)
2SO
3,B为(NH
4)
2SO
4,C为SO
2,D为NH
3,E为K
2SO
3,F为K
2SO
4,结合物质的性质解答该题.
点评:本题考查无机物的推断,题目难度中等,本题注意A可跟酸反应,又可与碱反应且A为正盐且为弱酸弱碱盐这一点,为解答该题的关键,也是易错点.

 NH3↑+H2O,
NH3↑+H2O, NH3↑+H2O;
NH3↑+H2O;