
按要求作答
(1)写出钠和水应的离子方式 ;
(2)写出氯化铝和氨水反应的化学方式 ;
(3)除去混入NaCl溶液中少量NaHCO3杂质的试剂是 ,离子方程式为 .
(4)除去Na2CO3粉末中混入的NaHCO3杂质用 方法,化学方程式为 .
考点:
化学方程式的书写;离子方程式的书写;钠的化学性质;钠的重要化合物.
专题:
几种重要的金属及其化合物.
分析:
(1)钠和水反应生成氢氧化钠和氢气;
(2)氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵;
(3)根据NaCl不能和盐酸反应而和K2CO3能与盐酸反应;
(4)根据Na2CO3加热不分解,NaHCO3加热分解.
解答:
解:(1)钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
(2)氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵;反应的化学方程式为:AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl,
故答案为:AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl;
(3)因NaCl不能和盐酸反应,NaHCO3能与盐酸反应反应生成氯化钠、水、二氧化碳,生成的氯化钠又溶于水,所以可用盐酸除去混入NaCl溶液中少量NaHCO3杂质,
故答案为:盐酸;HCO3﹣+H+=CO2↑+H2O;
(4)因Na2CO3加热不分解,NaHCO3加热分解得到碳酸钠、水、二氧化碳,所以可用加热的方法除去Na2CO3粉末中混入的NaHCO3杂质,
故答案为:加热;2NaHCO3 Na2CO3+CO2↑+H2O.
Na2CO3+CO2↑+H2O.
点评:
本题考查化学方程式、离子方程式书写方法和注意问题,反应的实质和产物判断是解题关键,题目较简单.注意(3)(4)除杂和分离的原则,需分析杂质和物质性质的不同,然后选择适当的试剂和方法.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
下列各组物质相互作用时,其中水既不作氧化剂,又不作还原剂,而反应仍属于氧化还原反应的是()
A. 氟与水反应 B. Na与水反应
C. 铝与强碱液作用 D. 过氧化钠与水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用有关胶体的观点解释的现象是( )
|
| A. | 在河流人海口处易形成三角洲 |
|
| B. | 在NaHCO3溶液中滴入CaCl2溶液,看不到沉淀 |
|
| C. | 少许FeCl3饱和溶液逐滴滴入沸水中,看不到红褐色沉淀 |
|
| D. | 同一支钢笔,同时使用不同牌号的墨水易发生堵塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
|
| A. | 分别加热这两种固体物质,并将生成的气体通入澄清石灰水中 |
|
| B. | 分别在这两种物质的溶液中,加入CaCl2溶液 |
|
| C. | 分别在这两种固体中,加入同浓度的稀盐酸 |
|
| D. | 分别在这两种物质的溶液中,加入少量澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH 溶液.过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为( )
|
| A. | 70% | B. | 52.4% | C. | 47.6% | D. | 30% |
查看答案和解析>>
科目:高中化学 来源: 题型:
3.84gFe和Fe2O3的混合物溶于过量盐酸中,生成0.03molH2,向反应后的溶液中加入KSCN检验,溶液无明显现象.求原混合物中Fe2O3的质量.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分子式为C12H12的物质A的结构简式为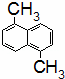 ,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有()
,其苯环上的二溴代物有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有()
A. 9种 B. 10种 C. 11种 D. 12种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n
B. 一种烃在足量的氧气中燃烧并通过浓硫酸,减少的总体积就是生成的水蒸气的体积
C. 某气态烃CxHy与足量O2恰好完全反应(温度>100℃),如果反应前后气体体积不变,则y=4
D. 相同质量的烃,完全燃烧,消耗O2越多,烃中含H量越高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学反应速率的说法正确的是()
A. 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B. 100mL2mol•L﹣1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C. SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
D. 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com