
下列离子方程式与所述事实相符且正确的是
A.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
B.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3= FeO42-+3Cl-+H2O+H+
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:2AlO2-+CO2+3H2O= 2Al(OH)3↓+CO32-
D.Ca(HCO3)2与过量 Ca(OH)2溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年江苏省高三12月学情调研化学试卷(解析版) 题型:填空题
(12分)工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(已知Cd的金属活动性介于Zn和Fe之间)
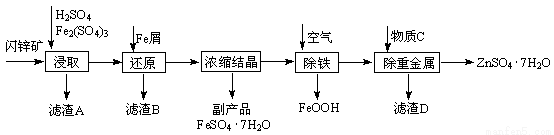
(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为 。
(2)浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为 。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为 。
该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是 。
(4)置换法除去重金属离子Cd2+,所用物质C为 。
(5)取28.70 g ZnSO4·7H2O加热至不同温度,剩余固体的质量变化如图所示。
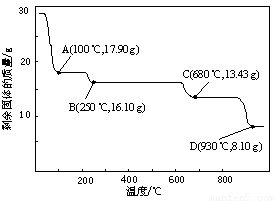
680℃时所得固体的化学式为 。
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4·H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省常州市高三上学期期末化学试卷(解析版) 题型:填空题
(12分)高氯酸钾广泛用于火箭及热电池业。实验室制取高氯酸钾的步骤为:称取一定质量的KCl、NaClO4溶解,然后混合,经冷却、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到。
有关物质溶解度与温度的关系如下表:

(1)写出实验室制取高氯酸钾的化学方程式: ;用蒸馏水多次洗涤晶体的目的是: 。
(2)Fe和KClO4反应放出的热量能为熔融盐电池提供550-660℃的温度,使低熔点盐熔化导电,从而激活电池,这类电池称为热电池。Li/FeS2热电池工作时,Li转变为硫化锂,FeS2转变为铁,该电池工作时,电池总反应为: 。
(3)Fe和KClO4作为热电池加热材料的供热原理为:KClO4 (s)+4Fe(s)= KCl (s)+ 4FeO(s),△H< 0。
①600℃时FeO可部分分解生成Fe3O4,写成有关的化学方程式: 。
②称取一定质量上述加热材料反应后的混合物(假定只含氯化钾一种钾盐)于烧杯中,用蒸馏水充分洗涤、过滤、干燥,固体质量减少了0.43g,在固体中继续加入过量的稀硫酸,微热让其充分反应,固体完全溶解得到的溶液中加入过量的NaOH溶液,经过滤、洗净、干燥,再在空气中充分灼烧得6.0 g棕色固体。求该加热材料反应前,铁和高氯酸钾的质量。(写出计算过程,结果保留2位有效数字) 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省常州市高三上学期期末化学试卷(解析版) 题型:选择题
下列溶液中有关微粒的物质的量浓度关系正确的是
A.物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,pH值的大小关系:②>①>③
B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)>(CH3COO-)>c(Cl-)=c(CH3COOH)>c(H+)=c(OH-)
C.常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7 mol·L-1
D.物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省常州市高三上学期期末化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA
B.常温常压下,28 g C2H4、CO的混合气体中含有碳原子的数目为1.5NA
C.常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA
D.标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省五市十校教研教改共同体高三第一次联考化学试卷(解析版) 题型:选择题
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示。下列判断正确的是

A.原溶液中一定含有Na2SO4
B.原溶液中一定含有的阴离子是OH-,CO32-,SiO32-,AlO2-
C.反应后形成的溶液溶质为NaCl
D.原溶液中含有CO32-与AlO2-的物质的量比为1:2
查看答案和解析>>
科目:高中化学 来源:2015-2015湖南省高二12月学科联赛化学试卷(解析版) 题型:填空题
(1)有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融硝酸钾 ⑥乙醇
⑦稀硫酸 ⑧金刚石 ⑨二氧化硫 ⑩冰醋酸。
属于非电解质的有_____;属于强电解质的有_____;(填序号)
(2)常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈 性,溶液中c(NH4+)与c(Cl-)的大小关系是:c(NH4+) c(Cl-);(填>,<或=)
(3)常温下,0.010mol·L-1盐酸和0.010mol·L-1氨水的pH之和 14,常温下,pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和 14(填>,<或=)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省益阳市高二1月月考化学试卷(解析版) 题型:填空题
Ⅰ.下表是几种电解质的电离常数(25℃)

(1)电解质的强弱顺序为__________________________________(用化学式表示,下同)。
(2)物质的量浓度相同的上述溶液,氢离子浓度最小的是______,溶质分子浓度最小的是_______。
(3)25℃时,在0.5 L 0.2 mol·L-1的HA溶液中,有0.01 mol的HA电离成离子。该温度下HA的电离常数K=________。
Ⅱ.已知下列弱酸的电离常数:H2CO3: Ka1=4.30×10-7 ;Ka2=5.61×10-11 H2SO3: Ka1=1.54×10-2;Ka2=1.02×10-7 HClO:Ka=2.95×10-8下列离子HCO3-、HSO3-、CO32-、ClO-、SO32-、在溶液中结合H+的能力由大到小的关系为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com