
 (1)写出化学式FNH3,
(1)写出化学式FNH3,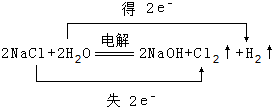 .
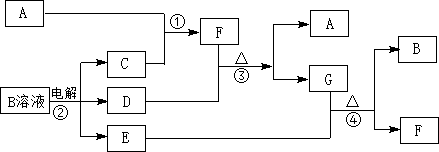
.分析 A、C、D是常见的气体单质,D为黄绿色,则D为Cl2,F气体有刺激性气味,极易溶于水,且液态常做致冷剂,结合G经常用作化学肥料,判断F为NH3;B电解生成气体单质C、D(氯气)、E,(3)中工业上电解B溶液制得一系列化工原料,可以推断是电解氯化钠溶液,则B为NaCl、C为H2、E为NaOH,结合转化关系可知,A为N2,G为NH4Cl,氯化铵与氢氧化钠反应可以得到氨气与NaCl,据此解答.
解答 解:A、C、D是常见的气体单质,D为黄绿色,则D为Cl2,F气体有刺激性气味,极易溶于水,且液态常做致冷剂,结合G经常用作化学肥料,判断F为NH3;B电解生成气体单质C、D(氯气)、E,(3)中工业上电解B溶液制得一系列化工原料,可以推断是电解氯化钠溶液,则B为NaCl、C为H2、E为NaOH,结合转化关系可知,A为N2,G为NH4Cl,氯化铵与氢氧化钠反应可以得到氨气与NaCl.
(1)由上述分析可知,F的化学式为:NH3,故答案为:NH3;
(2)鉴定NH4Cl中阳离子的实验方法和现象:取少量G的溶液加入试管中,用胶头滴管加入少量NaOH浓溶液,加热,用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色,说明含有铵根离子,
故答案为:取少量G的溶液加入试管中,用胶头滴管加入少量NaOH浓溶液,加热,用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色,说明含有铵根离子;
F为NH3,其电子式为: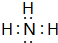 ,故答案为:
,故答案为: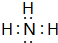 ;
;
(3)电解B溶液的化学方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑,标出电子转移的方向和数目为: ,
,
故答案为: ;
;
(3)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应离子方程式为2OH-+Cl2═ClO-+Cl-+H2O,反应④的离子方程式为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案为:2OH-+Cl2═ClO-+Cl-+H2O;NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
点评 本题考查无机框图的推断,“D气体在常温下呈黄绿色,F气体极易溶于水且液态常作制冷剂”是推断突破口,注意电解B溶液产物,熟练掌握中学常见化学工业,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 稀硝酸和碳酸钠 | B. | 氧化铜和稀硝酸 | C. | 碳和浓硫酸 | D. | 铜和浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO3)=0.4 mol/L | B. | c(SO2)=c(SO3)=0.15 mol/L | ||
| C. | c(O2)=0.35 mol/L | D. | c(SO2)+c(SO3)=0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
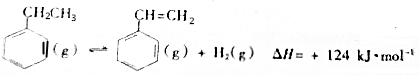
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | x | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀盐酸可除去烧瓶内残留的MnO2 | B. | 可用无色广口玻璃瓶保存氨水 | ||
| C. | 稀硝酸可除去试管内壁粘有的硫磺 | D. | 煮沸自来水可除去其中的Ca(HCO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
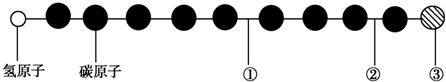
| A. | 该物质是烃的含氧衍生物 | B. | ①处的化学键是碳碳双键 | ||
| C. | ②处的化学键是碳碳单键 | D. | ③处的原子可能是氯原子或氟原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | X | Y | Z | R | T |
| 原子半径/nm | 0.037 | 0.077 | 0.074 | 0.186 | 0.102 |
| 主要化合价 | +1 | +4、-4 | -2 | +1 | +6、-2 |
| A. | X、Y、Z 位于同一周期 | |
| B. | R 与 Z 所形成的化合物均只含离子键 | |
| C. | 氢化物的沸点:Y<Z<T | |
| D. | 第一电离能:Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
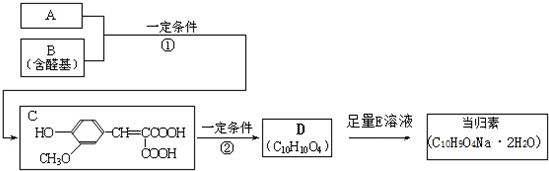
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com