
| A. | 按系统命名法,有机物 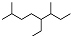 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 | |
| C. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 | |
| D. | 结构片段为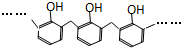 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 |
分析 A.该命名不满足取代基的编号之和最小原则;
B.烃CxHy完全燃烧耗氧量由(x+$\frac{y}{4}$)值决定;烃的含氧衍生物CxHyOz完全燃烧耗氧量由(x+$\frac{y}{4}$-$\frac{z}{2}$)值决定,据此判断;
C.苯和甲苯互为同系物,但苯不能使KMnO4酸性溶液褪色;
D.根据苯酚和甲醛发生缩聚反应.
解答 解:A.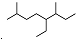 的命名中,取代基的编号之和不是最小的,说明编号方向错误,正确命名为2,6-二甲基-5-乙基辛烷,故A错误;
的命名中,取代基的编号之和不是最小的,说明编号方向错误,正确命名为2,6-二甲基-5-乙基辛烷,故A错误;
B.苯的x+$\frac{y}{4}$=6+$\frac{6}{4}$=7.5,即1mol苯消耗氧气7.5mol,苯甲酸的x+$\frac{y}{4}-\frac{z}{2}$=7+$\frac{6}{4}$-1=7.5,即1mol苯甲酸消耗氧气7.5mol,所以等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等,故B错误;
C.苯和甲苯互为同系物,但苯不能使KMnO4酸性溶液褪色,故C错误;
D.苯酚和甲醛发生缩聚反应得到酚醛树酯,结构片段
故选:D.
点评 本题主要考查了物质的命名、燃烧规律、物质的性质以及缩聚反应,需要注意的是酚醛发生缩聚反应的规律.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
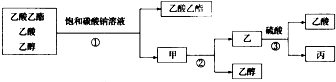 如图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图,实验过程中,所涉及的三次分离操作分别是( )
如图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图,实验过程中,所涉及的三次分离操作分别是( )| A. | ①蒸馏 ②过滤 ③分液 | B. | ①分液 ②蒸馏 ③过滤 | ||
| C. | ①蒸馏 ②分液 ③分液 | D. | ①分液 ②蒸馏 ③蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 例如:
例如: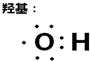
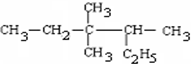 的名称3,3,4-三甲基己烷
的名称3,3,4-三甲基己烷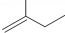 的名称2-甲基-1-丁烯.
的名称2-甲基-1-丁烯.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
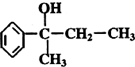 在工业上用基础的石油产品(乙烯、丙烯等)进行合成.合成A的过程可表示为:
在工业上用基础的石油产品(乙烯、丙烯等)进行合成.合成A的过程可表示为: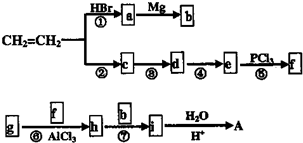
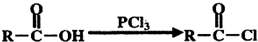
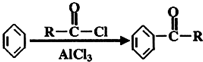
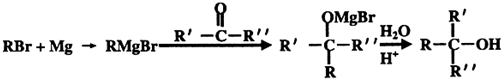
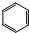 ;
;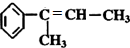 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PbO2是电池的负极 | |
| B. | 负极的电极反应式为:Pb(s)+SO42-(aq)-2e -=PbSO4(s) | |
| C. | 铅蓄电池属于一次电池 | |
| D. | 电池放电时,溶液酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镭的金属性比钙弱 | B. | 单质能与水反应生成氢气 | ||
| C. | 在化合物中呈+2价 | D. | 碳酸镭难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)
乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| X | Y | ||
| Z | W |
| A. | 原子半径由小到大的顺序为X<Z<Y<W | |
| B. | Y元素最高价氧化物对应的水化物化学式为HYO3 | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com