
【题目】下面关于硅的叙述中,正确的是( )
A.粗硅制备单晶硅不涉及氧化还原反应
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种短周期元素,A与B可形成BA型化合物,且A元素是卤族元素中非金属性最强的元素;金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8;C元素有3种同位素C1、C2、C3 , 其中自然界中含量最多的是C1 , C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍;D的气态氢化物的水溶液呈碱性,而其最高价氧化物对应的水化物为强酸;E元素为地壳中含量最多的元素。
(1)写出下列元素的元素符号:D , E。
(2)写出C1、C2、C3三种核素的符号:C1 , C2 , C3。
(3)E2-的离子结构示意图为。
(4)A与B形成的化合物的化学式是 ,
最常见的E与C2形成的分子中含个中子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:CO(g)+H2O(g)CO2(g)+H2(g),△H<0,在850℃,K=1,
(1)若升高到950℃,达到平衡时K1(填“大于”、“小于”或“等于”)
(2)在850℃,若向一容积可变的密闭容器中同时充入1molCO、3molH2O、1molCO2和xmol的H2: ①当x=5时,上述平衡向(填“正反应”或“逆反应”)方向进行
②若要使上述反应开始时向正反应方向进行,则x的取值为
③当x=5mol和x=6mol,上述反应达到平衡后,H2的体积分数分别为a%和b%,则a%b%(填“大于”、“小于”或“等于”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以如表和如图表示: 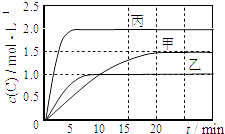
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物 | 1.5molA | 1.5molA | 6.0molA |
下列说法正确的是( )
A.x=1
B.10min内乙容器中反应的平均速率v(B)=0.025molL﹣1min﹣1
C.由图可知:T1<T2 , 且该反应为吸热反应
D.T1℃,起始时甲容器中充入0.5molA,1.5molB,平衡时A的转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“无论从经济的发展还是人类的进步而言,合成氨的发明都是本世纪科学领域中最辉煌的成就之一.”图1是与NH3相关的工业过程示意图. 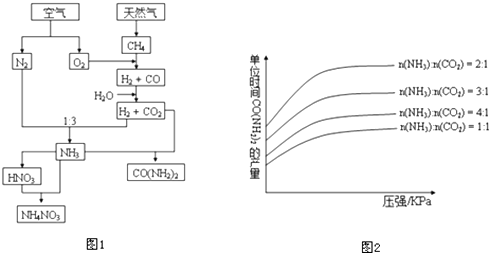
已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890kJmol﹣1
2CO(g)+O2(g)═2CO2(g)△H=﹣566.0kJmol﹣1
2H2(g)+O2(g)═2H2O(g)△H=﹣571.6kJmol﹣1
(1)请写出CH4(g)与O2(g)反应生成CO(g)和H2(g)的热化学反应方程式 .
(2)在生产过程中,会涉及H2和CO2的分离.你认为可取的方法是(填序号).
a.在加压条件下用水吸收CO2 b.用NaOH溶液吸收CO2 c.加压,使CO2液化
(3)合成尿素的反应是分作两步进行的:
①CO2(g)+2NH3(g)═H2NCOONH4(aq) (氨基甲酸铵)△H=﹣159.47kJmol﹣1
②H2NCOONH4(aq)═CO(NH2)2(aq)+H2O(l)△H=﹢28.49kJmol﹣1
在生产条件下,单位时间内获得尿素的产量与压强和n(NH3):n(CO2)的关系如图2所示.生产过程中n(NH3):n(CO2)的最佳配比为 , 而实际生产条件下,往往使n(NH3):n(CO2)≥3,这是因为、 . 在得到的尿素溶液中会含有少量的氨基甲酸铵,除去这种杂质最简便的方法是 .
(4)将氨分为两部分,一部分经逐级氧化吸收转化为硝酸,另一部分又与HNO3反应生成NH4NO3 . 若HNO3与NH3的反应是完全的,有标准状况下50LNH3经上述反应过程生成84g NH4NO3 . 则NH3逐级转化为HNO3的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将相同质量的两块铜片分别和浓硝酸、稀硝酸(两者均过量)反应,下列叙述正确的是( )
A.反应速率:两者相同
B.消耗HNO3的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其他元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。
根据以上信息,回答下列问题。
(1)A和D的氢化物中,沸点较低的是(选填“A”或“D”);A和B的离子中,半径较小的是(填离子符号)。
(2)元素C在元素周期表中的位置是。
(3)A和E可组成离子化合物,其晶胞结构如上图所示,阳离子(用“”表示)位于该正方体的顶点和面心,阴离子(用“o”表示)均位于小正方体中心。该化合物的电子式是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com