
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
. .
. ,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
,该化合物是由极性(填“极性”或“非极性”)共价键形成的. 分析 由元素在周期表中的相对位置可知:①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,
(1)稀有气体化学性质稳定;
(2)上述元素中高氯酸为含氧酸中酸性最强的酸,KOH的碱性最强;
(3)氧化物中氧化铝为两性氧化物;
(4)④与⑥形成化合物为Na2S;
(5)①与⑦形成的化合物为CCl4.
解答 解:由元素在周期表中的相对位置可知:①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,
(1)这些元素中,化学性质最不活泼的是Ar,故答案为:Ar;
(2)上述元素中高氯酸为含氧酸中酸性最强的酸,其化学式为HClO4,KOH的碱性最强,其电子式为 ,
,
故答案为:HClO4; ;
;
(3)氧化物中氧化铝为两性氧化物,则最高价氧化物是两性氧化物的元素是Al,故答案为:Al;
(4)④与⑥形成化合物为Na2S,电子式表示化合物的形成过程为
故答案为: ;
;
(5)①与⑦形成的化合物为CCl4,为共价化合物,各原子满足8电子稳定结构,电子式为
故答案为:
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、性质、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意化学用语的使用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.25mol/L | B. | 0.44mol/L | C. | 0.5mol/L | D. | 0.8mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白、红、白、蓝 | B. | 白、白、白、蓝 | C. | 白、黑、白、蓝 | D. | 红、黑、红、蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
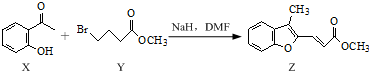
| A. | 物质X在空气中不易被氧化 | |
| B. | 物质Y中只含1个手性碳原子 | |
| C. | 物质Z中所有碳原子可能在同一平面内 | |
| D. | 等物质的量的X、Y分别与NaOH反应,最多消耗NaOH的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有离子键,可能含共价键,共价化合物中只含共价键绝不含有离子键 | |
| B. | 单质分子中均存在化学键,且只含有共价键,不可能含有离子键 | |
| C. | 共价化合物中可能含非极性共价键,离子化物中不可能含非极性共价键 | |
| D. | 共价化合物中可能含离子键,离子化合物中只含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
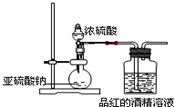 为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)
为探究SO2的漂白是SO2直接作用于有色物质,还是SO2与水反应的产物的作用,设计如图装置进行实验:(图中所用硫酸的质量分数为70%)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
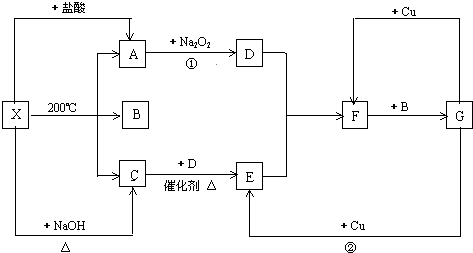
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com