
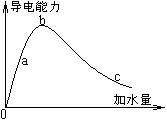
在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力如图所示,请回答:
(1)“0”点导电能力为0的理由 。
(2)a、b、c三点溶液的pH值由小到大的顺序为 。
(3)a、b、c三点中电离度最大的是: 。
(4)若使c点溶液中[CH3COO![]() ]增大,溶液的pH也
]增大,溶液的pH也
增大,可采取的措施为:① ;② ;③ 。
(1)由于醋酸为共价化合物,在固、液态时不存在离子,也就谈不上存在自由移动的离子,所以不导电。 (2)b < a < c ; (3)c ; (4)加NaOH(固);Mg ;Na2CO3(固)。
|
冰醋酸加水稀释的过程中,醋酸电离生成氢离子和醋酸根离子,随着氢离子和醋酸根离子浓度的变化,其导电能力也发生变化。从导电能力上看,b点强于a点、a点强于c点,说明溶液中自由移动的离子浓度b  
练习册系列答案
 阅读快车系列答案 阅读快车系列答案
相关习题
科目:高中化学 来源: 题型:  在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.请回答: 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.请回答:(1)“O”点导电能力为0的理由是 在“O”点处醋酸未电离,无离子存在 在“O”点处醋酸未电离,无离子存在 ;(2)a、b、c三点处,溶液的c(H+)由小到大的顺序为 c<a<b c<a<b ;(3)a、b、c三点处,电离程度最大的是 c c ;(4)若使c(CH3COO-)增大,溶液c(H+)减小,可采取的措施是:① 加少量NaOH固体 加少量NaOH固体 ;②加少量Na2CO3固体 加少量Na2CO3固体 ;③加入Zn、Mg等金属 加入Zn、Mg等金属 .查看答案和解析>> 科目:高中化学 来源: 题型:  在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示,请回答: 在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示,请回答:(1)写出醋酸的电离方程式 CH3COOH?CH3COO-+H+ CH3COOH?CH3COO-+H+ .(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为 b>a>c b>a>c .(3)a、b、c三点中醋酸的电离程度最大的是 C C .(4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲 < < 10C(H+)乙(填“大于”、“小于”或“等于”)甲,其原因是:醋酸溶液越稀电离程度越大 醋酸溶液越稀电离程度越大 .查看答案和解析>> 科目:高中化学 来源: 题型: (14分)、根据电离平衡移动原理完成下列表格 (1)已知:CH3COOH为弱电解质,在醋酸溶液中,当改变条件后,完成表格中的变化情况
(2)在一定温度下,冰醋酸加水稀释过中溶液的导电能力如下图所示,请回答: ①写出醋酸的电离方程式________________。 ②a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________。 ③a、b、c三点中醋酸的电离程度最大的是 。 ④取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲_____10C(H+)乙(填“大于”、“小于”或 “等于”),
查看答案和解析>> 科目:高中化学 来源:2012届浙江省台州市高二下学期期末测试化学 题型:选择题 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如下图所示。下列说法不正确的是
A.在0点时,醋酸不导电 B.a、b、c三点,a点时醋酸溶液中H+浓度最小 C.b点时,醋酸电离程度最大 D.可通过微热的方法使c点溶液中c(CH3COO-)增大
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |