
| A. | CH3CH2CH2CH2CH2OH | B. | (CH3)2COHCH2CH3 | ||
| C. | (CH3)2CHCH2CH2OH | D. | (CH3)3CCH2OH |
分析 能跟H2加成生成2-甲基丁烷,说明Y和Z均为分子中含5个C原子的不饱和烃,其碳骨架为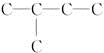 .氯代烃发生消去反应生成烯烃和烯烃加氢生成烷烃,碳架不变,故化合物X的碳架有一个支链甲基,以此解答该题.
.氯代烃发生消去反应生成烯烃和烯烃加氢生成烷烃,碳架不变,故化合物X的碳架有一个支链甲基,以此解答该题.
解答 解:能跟H2加成生成2-甲基丁烷,说明Y和Z均为分子中含5个C原子的不饱和烃,其碳骨架为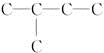 .氯代烃发生消去反应生成烯烃和烯烃加氢生成烷烃,碳架不变,故化合物X的碳架有一个支链甲基,
.氯代烃发生消去反应生成烯烃和烯烃加氢生成烷烃,碳架不变,故化合物X的碳架有一个支链甲基,
A.CH3CH2CH2CH2CH2OH没有支链,故A错误;
B.(CH3)2COHCH2CH3对应X为(CH3)2CClCH2CH3,生成的烯烃有2种,符合题目要求,故B正确;
C.(CH3)2CHCH2CH2OH对应的X发生消去反应生成一种烯烃,故C错误;
D.(CH3)3CCH2OH对应的X为(CH3)3CCH2Cl,不能发生消去反应,故D错误.
故选B.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能力的考查,熟悉卤代烃消去的规律和烯烃的加成特点是解题的关键,难度不大.


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
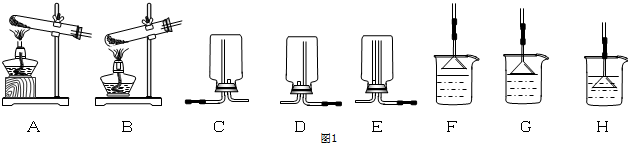
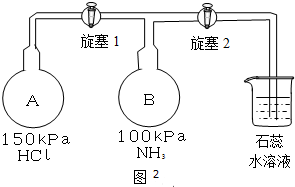
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
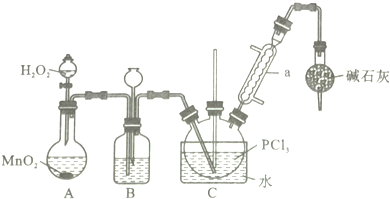
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| PCl3 | -112.0 | 76.0 | 137.5 | 均为无色液体,遇水均剧烈水解为含氧酸和氯化氢,两者互溶 |
| POCl3 | 2.0 | 106.0 | 153.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应为还原反应 | |
| B. | 上述反应中若产生0.1mol SO42-,则消耗SO2的物质的量为0.1mol | |
| C. | Fe2(SO4)3、品红两种溶液都能使上述反应进行 | |
| D. | 通入Cl2会增强SO2的漂白作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用10ml量筒量取7.5ml稀盐酸 | |
| B. | 用托盘天平称取25.20gNaCl晶体 | |
| C. | 用蒸发结晶的方法由硫酸铜溶液制取蓝帆 | |
| D. | 用100ml容量瓶配置0.5mol/l的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将该Na2CO3 溶液转移至250ml容量瓶中,加蒸馏水稀释至刻度线,摇匀 | |
| B. | 将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取150ml蒸馏水加入,搅拌 | |
| C. | 将该Na2CO3 溶液转移至250ml烧杯中,用量筒量取400ml蒸馏水加入,搅拌 | |
| D. | 将该Na2CO3 溶液转移至500ml容量瓶中,加蒸馏水稀释至刻度线,摇匀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com