


 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
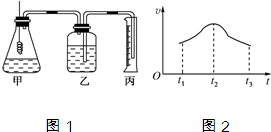
| ʵ����� | ���� ����/g | ����״̬ | C��H2SO4�� /mol?L-1 | V��H2SO4�� /mL | ��Һ�¶�/�� | ������ʧ��ʱ��/s | |
| ��Ӧǰ | ��Ӧ�� | ||||||
| 1 | 0.10 | ˿ | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | ��ĩ | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | ˿ | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.10 | ˿ | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.10 | ��ĩ | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.10 | ˿ | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.10 | ˿ | 1.0 | 50 | 35 | 50 | 50 |
| 8 | 0.10 | ˿ | 1.1 | 50 | 20 | 34 | 100 |
| 9 | 0.10 | ˿ | 1.1 | 50 | 20 | 44 | 40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| O2 |
| O2 |
| H2O |
| A���٢� | B���ۢ� |
| C���٢ڢ� | D���٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe��ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | ||||
| B��Na2O2����ˮ����O2��Na2O2+H2O�T2Na++2OH-+O2�� | ||||
C����ʯī���缫��ⱥ��MgCl2��Һ��2Cl-+2H2O
| ||||
| D��ǿ����Һ��NaClO��Fe��OH��3��Ӧ����Na2FeO4��4OH-+3ClO-+2Fe��OH��3�T2FeO42-+3Cl-+5H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ƭ�϶�ͭʱ������������3.2g������Һ��ͨ���ĵ��ӵ����ʵ���Ϊ0.1mol |
| B�������绯ѧ��ʴ������������Ҫ��������ˮĤ��PH��ͬ������ĸ�����Ӧ��ͬ |
| C���μӷ�Ӧ�����ʵ������Ǿ�����ѧ��Ӧ���ʵ���Ҫ���� |
| D����ⱥ��ʳ��ˮ���ռ�������ӽ���Ĥ�����ɷ�ֹ������������Cl2���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
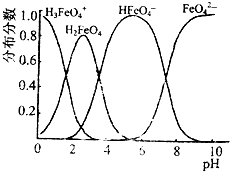 �������ƵĻ�ѧʽΪNa2FeO4����Ҫ��ش��������⣺
�������ƵĻ�ѧʽΪNa2FeO4����Ҫ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��SO3��HSO4- |
| B��MnO4-��Mn2+ |
| C��PCl3��PCl5 |
| D��CO2��H2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��v��A��=0.15 mol?L-1?min-1 |
| B��v��B��=0.015 mol?L-1?s-1 |
| C��v��C��=0.40 mol?L-1?min-1 |
| D��v��D��=0.45 mol?L-1?min-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com