
| A. | 无论乙烯与丙烯酸以何种比例混合,只要二者总物质的量是个定值,完全燃烧时所消耗的氧气也一定是个定值 | |
| B. | 鉴别甲苯、苯乙烯、苯酚、丙烯酸溶液可选用KMnO4溶液、溴水 | |
| C. | 苯中的少量苯酚可先加适量的浓溴水,使苯酚生成三溴苯酚,再过滤而除去 | |
| D. | 苯酚的酸性很弱,但可以和Na2CO3反应 |
分析 A、各组混合物无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量是定值,则1mol各组分消耗氧气的物质的量相等;
B、甲苯、苯乙烯、苯酚、丙烯酸溶液都能够使KMnO4溶液褪色;
C、三溴苯酚能够溶于苯;
D、苯酚的酸性强于碳酸氢根离子.
解答 解:A、C2H5COOH可以改写为C3•3H2O,故1mol的CH2=CH2、C2H5COOH消耗氧气都是3mol,消耗氧气相等,故A正确;
B、甲苯、苯乙烯、苯酚、丙烯酸溶液都能够使KMnO4溶液褪色,苯乙烯、丙烯酸溶液都能够使溴水褪色,无法鉴别,故B错误;
C、三溴苯酚能够溶于苯,无法除掉,故C错误;
D、苯酚的酸性强于碳酸氢根离子,所以苯酚能够与碳酸钠溶液反应生成苯酚钠和碳酸氢钠,故D正确;
故选BC.
点评 本题考查了有机物燃烧耗氧量的计算、有机物的鉴别、苯酚的酸性、相似相溶,注意三溴苯酚能够溶于苯,题目难度不大.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题
| 浓度/mol.L-1 | NO | N2 | CO2 |
| 时间/min | |||
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.30 | 0.030 |
| 30 | 0.040 | 0.30 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性 X>Y | |
| B. | Y单质与Z的最高价氧化物对应的水化物反应可制备氢气 | |
| C. | Y的最高价氧化物对应的水化物能溶于氢氧化钠 | |
| D. | 一定条件下,Z单质与W的常见单质直接生成ZW2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在CH2=CH2分子中,存在五个s-sp2σ键和一个π键 | |
| B. | N、O、F电负性大小:F>O>N;第一电离能大小:F>O>N | |
| C. | 酸性强弱:H2SO4>H2SO3>H2SeO3;岩浆晶出的先后顺序:SiO2、MgSiO3、CaSiO3 | |
| D. | 在共价化合物中,一定存在极性共价键,可能存在非极性共价键,一定不存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
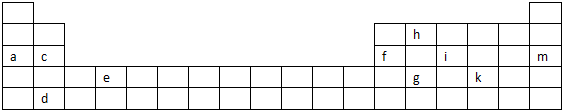
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
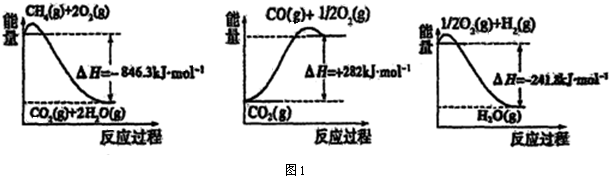
| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Kb=1.77×10-5 |
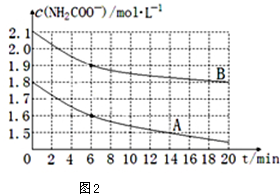
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com