
| △c |
| △t |
| △c |
| △t |
| 0.5mol?L-1 |
| 5min |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3+H2O=H2SO4 | ||||
B、NH4Cl
| ||||
| C、2Na+2H2O=2NaOH+H2↑ | ||||
| D、NaOH+HNO3=NaNO3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、失去电子的物质是还原剂,具有氧化性 |
| B、氧化还原反应的本质是元素化合价的升降 |
| C、氧化还原反应中,某元素由化合态变为游离态,此元素可能被还原或被氧化 |
| D、在氧化还原反应中,电子不可以在同种元素间转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
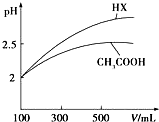 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | ①往试管中滴入几滴 |
②继续滴入几滴新制氯水 |
| 现象 | 溶液无明显变化 | 溶液显红色 |
| 原因 | 溶液中没有Fe3+ | (用简要文字说明原因) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 L 2 mol?L-1的(NH4)2S溶液中含有的S2-数目为0.2NA |
| B、7.8g苯中含有C=C键数目为0.3NA |
| C、常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA |
| D、用惰性电极电解1 L浓度均为2 mol?L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,理论上阴极析出6.35g金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com