
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-270 kJ·mol-1,下列说法错误的是
A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量
B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ
C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸气的能量
D.2个氢气分子与1个氧气分子反应生成2个水蒸气分子放出270kJ热量
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期期中化学试卷(解析版) 题型:填空题
在773 K,体积为V L的恒温恒容的容器中,硫和氧气可以发生如下转化,其反应过程和能量的关系如图1所示。其中状态III为平衡状态。
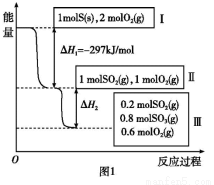
已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ/mol。
2SO3(g) ΔH=-196.6 kJ/mol。
请回答下列问题:
(1)写出表示硫的燃烧热的热化学方程式: 。
(2)状态II到状态III放出的热量为 。
(3)在另一个温度和容积相同的容器中,1 mol SO2和2 mol O2充分反应,放出的热量比∣ΔH2∣ (填“大”、“小”或“相等”)。
(4)恒容条件下,对状态III采取下列措施,能使n(SO3)/n(SO2)增大的有 。
A.降低温度
B.充入He气
C.再充入1 mol SO2(g)和1 mol O2(g) D.使用催化剂
(5)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是 。
(6)图2中表示平衡混合物中SO3的含量最高的一段时间是 。
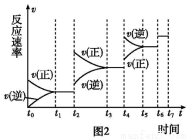
A. t1~t2 B. t3~t4 C. t5~t6 D. t6~t7
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省龙岩四校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.NaOH溶液能导电,所以NaOH溶液是电解质
B.固体KC1不导电,但KC1是电解质
C.氯水能导电,所以Cl2是电解质
D.C02的水溶液能导电,所以C02是电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:实验题
中和热的测定实验(如图)。
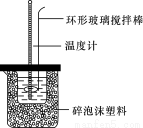
(1)量取反应物时,取50 mL 0.50 mol·L-1的盐酸,还应加入的试剂是________(填序号)。
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(2)在实验过程中,该同学需要测定并记录的实验数据有_____________(填序号)。
A.盐酸的浓度
B.盐酸的温度
C.氢氧化钠溶液的浓度
D.氢氧化钠溶液的温度
E.水的比热容
F.溶液混合后的最高温度
(3)若用50 mL 0.5 mol·L-1醋酸溶液代替上述盐酸测定中和热,所得数据_____________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
下列有关反应热的说法中正确的是
A.一个化学反应是否能在常温下发生与该反应的ΔH值的大小没有必然联系
B.中和热ΔH=-57.3 kJ·mol-1,所以1.00 L 1.00 mol·L-1 H2SO4与稀的NaOH溶液恰好完全反应放出57.3 kJ的热量
C.用等体积的0.50 mol·L-1盐酸、0.55 mol·L-1 NaOH溶液进行中和热测定的实验,会使测得的值偏大
D.在101 kPa时,1 mol CH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:计算题
配制350mL1.0mol/LH2SO4溶液,需用98%的浓硫酸溶液(ρ=1.84g/L)体积为多少?取25 mL1.0mol/LH2SO4溶液与2g锌粉充分反应,产生标准状况下H2多少升?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是 ( )
选项 | 微 | 所加试剂 | 离子方程式 |
A | NH | 少量Ba(OH)2溶液 | 2NH = BaSO4↓+NH3·H2O |
B | Mg2+、HCO | 过量NaOH溶液 | Mg2++2HCO = MgCO |
C | H+、Na+、NO | Fe粉 | Fe+2H+= Fe2++H2↑ |
D | Ca2+、NH3·H2O、Cl- | 通入过量CO2 | NH3·H2O+CO2 = NH |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:填空题
①22 g CO2所含的分子数为 个,所含原子个数与标准状况下 LCH4所含原子个数相同。
②标准状况下,560mL某气体A的质量为0.75g,则其摩尔质量为 ;已知该气体在水中的溶解度为448(气体溶解度指该气体在压强为101kPa,0℃时,溶解在1体积水里达到饱和状态时的气体的体积),则得到的饱和溶液中溶质A的质量分数为 (A不与水反应),若测得该溶液密度为1.24g/cm3,则该溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:实验题
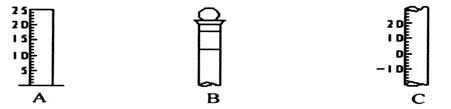
(1)请写出下列仪器的名称:A ,B ,C 。
(2)仪器B上标记有 (填序号)。
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
Ⅱ.现用98%的浓H2SO4(密度为1.84g/cm3)来配制480mL0.2mol/L的稀H2SO4。
有关操作为:①计算所需浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释、冷却 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题
(3)应用量筒量取的浓硫酸体积是 mL,实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有 。
(4)第③步中稀释浓硫酸的操作是 。
(5)将所配制的稀H2SO4进行测定,发现实际浓度大于0.2mol/L。请你分析下列哪些操作会引起所配浓度偏大(填写字母) 。
A.用量筒量取浓硫酸时,仰视量筒的刻度 |
B.容量瓶未干燥即用来配制溶液 |
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容 |
D.往容量瓶转移时,有少量液体溅出 |
E.烧杯未进行洗涤
F.在容量瓶中定容时俯视容量瓶刻度线
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com