
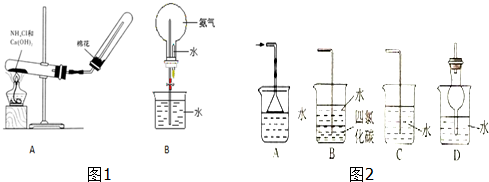
分析 (1)氯化铵和氢氧化钙固体加热制取氨气;
(2)根据氨气的喷泉实验原理回答,滴有酚酞的溶液变红,溶液显示碱性;
(3)氨气溶于水生成一水合氨;
(4)选择的装置必须能够防止倒吸.
解答 解:(1)实验室制取氨气是用氯化铵和氢氧化钙固体加热生成氨气和氯化钙、水,其化学方程式是:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O;
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O;
(2)氨气极易溶于水,可以完成喷泉实验,氨水是弱碱,能够电离出氢氧根离子,致使酚酞溶液显红色,故答案为:红色喷泉;氨气极易溶于水;溶于水显碱性;
(3)氨气溶于水生成一水合氨,一水合氨电离生成铵根和氢氧根,化学反应方程式为:NH3+H2O?NH3•H2O?NH4++OH-,故答案为:NH3+H2O?NH3•H2O?NH4++OH-;
(4)因为氨气极易溶于水,吸收多于的氨气装置,必须能够防止倒吸,AD装置中的倒置的漏斗和球形干燥管的体积较大,能防止液体倒吸进入反应装置,
B装置中四氯化碳可以减慢氨气溶于水的速率,故答案为:ABD.
点评 本题考查了氨气的制取和性质检验,涉及了实验装置的选择、化学方程式的书写,本题难度不大.


科目:高中化学 来源: 题型:选择题
| A. | V(O2)=0.01mol/L•s | B. | V(NO)=0.008mol/L•s | ||
| C. | V(H2O)=0.003mol/L•min | D. | V(NH3)=0.002mol/L•s |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和NaOH溶液 | B. | NO2和水 | C. | NH3和水 | D. | Cl2和NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用 NaHCO3 溶液可一次鉴别出稀盐酸、NaOH溶液、AlCl3溶液、NaAlO2 溶液 | |
| B. | 高锰酸钾试剂瓶内壁上黑色物质可用稀盐酸洗涤 | |
| C. | 除去SO2 中少量HCl,将其通入饱和的Na2SO3 溶液 | |
| D. | 将硝酸铵晶体溶于水,测得水温下降,证明硝酸铵水解是吸热的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com