
【题目】相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
A.若分子数相等,则体积相等
B.若原子数相等,则中子数相等
C.若质量相等,则质子数相等
D.若体积相等,则质量数相等
【答案】A
【解析】解:相同状况下的两种气体12C18O和14N2 , 计算其摩尔质量M(12C18O)=30g/mol,M(14N2)=28g/mol, A.依据阿伏伽德罗定律内容可知,同温、同压、同体积的气体,气体物质的量相同,所含分子数相同,若两种气体的分子数相同,则体积相同,故A正确;
B.若两种气体的原子数相等,则两种气体的分子数也相同,由于一个12C18O分子和一个14N2分子中的中子数不同,所以,两种气体的中子数不相等,故B错误;
C.若两种气体质量相等,因为分子的相对分子质量不同,分子质量不同,分子的个数不同,又因为每个分子中含有相同的质子数是14,所以,两种气体的质子数不相等,故C错误;
D.若两种气体体积相等,气体物质的量相同,M(12C18O)=30g/mol,M(14N2)=28g/mol,两者质量数不相等,故D错误;
故选A.
12C18O和14N2的分子构成,一个12C18O分子是由一个12C原子和一个18O原子构成,12C原子内有6个质子,6中子,18O原子内有8个质子和10个中子,一个12C18O分子中有14个质子、16个中子,相对分子质量是30;
一个14N2分子是由2个14N原子构成,14N原子内有7个质子和7个中子,一个14N2分子中有14个质子和14个中子,相对分子质量是28.
A.相同条件下,气体分子数目之比等于气体体积之比;
B.NO和N2都是双原子分子,若原子数相等,则分子数相等,但中子数不相等;
C.NO和N2的摩尔质量不相等,根据n= ![]() 可知,等质量的12C18O和14N2的物质的量不相等;
可知,等质量的12C18O和14N2的物质的量不相等;
D.相同条件下,气体分子数目之比等于气体体积之比.


科目:高中化学 来源: 题型:
【题目】开发新能源是解决环境污染的重要举措,其中甲醇、乙醇、甲烷都是优质的清洁燃料,可制作燃料电池。
(1)已知:①C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH1=-1366.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0kJ/mol
③H2O(g)=H2O(l) ΔH3=-44 kJ/mol。
乙醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:______________________。
(2)可利用甲醇燃烧反应设计一个燃料电池。如下图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
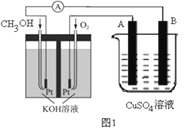
①写出燃料电池负极的电极反应式_________________。
②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是_______极(填“A”或“B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为________L。
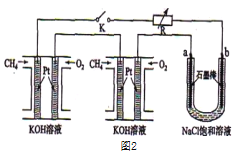
(3)某研究小组将两个甲烷燃料电池串联后如上图2作为电源,进行饱和氯化钠溶液电解实验若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量表达式为_____________(法拉第常数F=9.65×l04C/ mol),最多能产生的氯气体积为_____L(标准状况)。
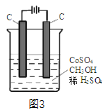
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+在阳极氧化成Co3+,生成的Co3+将甲醇氧化成CO2和H+(用石墨烯除去Co2+),现用如图3所示装置模拟上述过程,则Co2+在阳极的电极反应式为________________________除去甲醇的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW,该温度下,将浓度为amol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A. a=b
B. 混合溶液的pH=7
C. 混合溶液中,c(H+)=![]() mol·L-1
mol·L-1
D. 混合溶液中c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题: 
(1)该混合液中含溶质MgCl2的物质的量为 ,
(2)将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(化学式用H2B表示)在水中的电离方程式是H2B===H++HB-;HB-![]() H++B2-。回答下列问题。
H++B2-。回答下列问题。
(1)Na2B溶液显_____(填“酸性”、“中性”或“碱性”),理由是_______(用离子方程式表示)。
(2)在0.1 mol·L-1的Na2B溶液中,下列粒子浓度关系式正确的是____。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
D.c(Na+)=2c(B2-)+2c(HB-)
(3)已知0.1 mol·L-1 NaHB溶液的pH=2,则0.1 mol·L-1 H2B溶液中的氢离子的物质的量浓度可能____0.11 mol·L-1(填“<”、“>”或“=”),理由是_____。
(4)0.1 mol·L-1 NaHB溶液中各种离子浓度由大到小的顺序是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
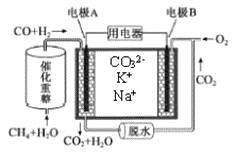
A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol e-
3H2+CO,每消耗1molCH4转移12mol e-
B. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
C. 电池工作时,CO32-向电极B移动
D. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应速率相同的是
A.使用催化剂和不使用催化剂
B.镁、铝与同浓度盐酸反应
C.大理石块和大理石粉与同浓度盐酸反应
D.0.1 mol/L硫酸和0.2 mol/L盐酸与同浓度的氢氧化钠溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是化学研究的重要方法,下列物质分类错误的是()
A.化合物:干冰、明矾、烧碱B.同位素:石墨、C60、金刚石
C.混合物:漂白粉、纯净矿泉水、盐酸D.非电解质:乙醇、四氯化碳、甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X溶液中可能含有下列8种离子中的几种:Fe3+、Fe2+、Na+、NH4+、CO32、Cl、SO32、SO42。某同学为确定其成分,设计并完成以下实验(不考虑水解,所加试剂均足量):
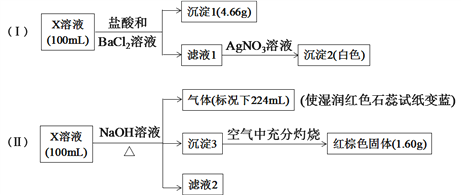
下列说法正确的是
A. X溶液中一定存在Na+、SO32、SO42、CO32
B. X溶液中一定存在NH4+、Na+、SO42,至少含有Fe3+、Fe2+离子中的一种
C. 取少量X溶液,先加入适量氯水,再加少量KSCN溶液,若溶液呈血红色,则含有Fe2+
D. X溶液中一定含有Cl,且c(Cl)≥0.1mol·L1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com