


科目:高中化学 来源: 题型:
| A、在pH=11的溶液中,水电离出的c(OH-)一定等于10-3mol/L |
| B、将pH=1的酸和pH=13的碱溶液等体积混合后,溶液的pH一定等于7 |
| C、一元酸HA与一元碱BOH混合后,溶液中c(A-)=c(B+),则溶液呈中性 |
| D、若强酸、强碱中和后溶液的pH=7,则中和之前酸、碱的pH之和一定等于14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用NaOH溶液可以除去乙酸乙酯中的乙酸 |
| B、乙烯和苯都能与溴水反应而使溴水褪色 |
| C、用新制的银氨溶液可区分甲酸甲酯和乙醛 |
| D、脂肪、糖类和蛋白质都是人体重要的营养物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na在氧气中燃烧主要生成Na2O |
| B、将SO2通入CaCl2溶液可生成CaSO3沉淀 |
| C、将CO2通入次氯酸钙溶液可生成次氯酸 |
| D、将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、四种元素的原子半径:A<B<C<D |
| B、四种元素A、B、C、D的氧化物都不止一种 |
| C、由B与A组成的化合物的沸点一定低于由C与A组成的化合物的沸点 |
| D、CaA2、CaB2这两种化合物中,阳离子与阴离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y |
| Z |
| A、①②③④ | B、①②④ |
| C、②④ | D、①② |
查看答案和解析>>
科目:高中化学 来源: 题型:
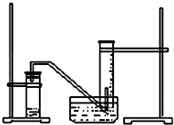 某学生利用锌与稀硫酸反应产生的氢气的体积,粗略测定锌的摩尔质量(设Wg锌片全部反应,产生气体的体积折算成标准状况时不超过50mL).实验装置如图请回答:(1)进行此试验时,必须保证气密性良好,如何检验此装置的气密性?
某学生利用锌与稀硫酸反应产生的氢气的体积,粗略测定锌的摩尔质量(设Wg锌片全部反应,产生气体的体积折算成标准状况时不超过50mL).实验装置如图请回答:(1)进行此试验时,必须保证气密性良好,如何检验此装置的气密性?查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com