
【题目】下列说法没有科学性错误的是
A.“白雪牌”漂白精可令所有有色物质黯然失“色”,没有最白,只有更白
B.液态氯化氢是100%的盐酸,其H+浓度极大
C.氯元素有毒,禁入口中
D.CaCl2具有吸水性和潮解性,夏日里用CaCl2的水溶液喷洒柏油路,可有效保护路面
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
A.
图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.
图中曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化
C.
图③表示10 mL 0.01 molL﹣1 KMnO4 酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.
图中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液与人类生活息息相关,请回答下列问题
(1)某温度下,Kw=1×10﹣12( molL﹣1)2 , 若保持温度不变,向水中滴入稀硫酸恰好使溶液中c(H+)/c(OH﹣)=1×1010 , 则此时水电离出的c(H+)=molL﹣1 .
(2)常温下若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是 .
A.若混合后溶液呈中性,则c(H+)+c(OH﹣)=2×10﹣7mol/L
B.若V1=V2 , 混合后溶液的pH一定等于7
C.若混合后溶液呈酸性,则V1一定大于V2
D.若混合后溶液呈碱性,则V1一定小于V2
(3)下列曲线中,可以描述乙酸(甲,Ka=1.8×10﹣5 mol/L)和一氯乙酸(乙,Ka=1.4×10﹣3 mol/L)在水中的电离度与浓度关系的是 
(4)在下列实验中,能证明醋酸酸性比盐酸酸性弱的是 .
A.将等体积、pH=4的盐酸和醋酸稀释成pH=5的溶液,测量所需加入水量的多少
B.向等体积、等pH的盐酸和醋酸中分别加入同量的相应钠盐固体,测溶液的pH有无变化
C.向等体积、等浓度的盐酸和醋酸分别加入足量锌粉,测量产生氢气的体积
D.用等体积、等浓度的盐酸和醋酸做导电性实验,根据灯泡的明亮程度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应C(s)+H2O(g)H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图. 
①图中t2到t3段、t4到t6段时引起平衡移动的条件分别可能是、;
②图中表示平衡混合物中CO的含量最高的一段时间是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的化学方程式书写及反应类型判断均正确的是( )
A.甲烷与氯气反应:CH4+Cl2 ![]() CH3Cl+HCl(加成反应)
CH3Cl+HCl(加成反应)
B.乙烯与水在一定条件下生成乙醇:CH2=CH2+H2O ![]() C3CH2OH(加成反应)
C3CH2OH(加成反应)
C.麦芽糖制葡萄糖: ![]() +H2O
+H2O ![]() (氧化反应)
(氧化反应)
D.乙醛与银氨溶液反应:CH3CHO+2Ag(NH3)2OH ![]() CH3COONH4+3NH3+2Ag↓+H2O(取代反应)
CH3COONH4+3NH3+2Ag↓+H2O(取代反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂,某化学小组的同学在老师的指导下制备氢化钙.
【查阅资料】
Ⅰ.金属Ca的部分性质有:
①常温或加热条件下Ca都能与氧气反应;
②Ca常温遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热;
③Ca+H2 ![]() CaH2(固体)
CaH2(固体)
Ⅱ.固体CaH2的部分性质有:
①常温:CaH2+2H2O=Ca(OH)2+2H2↑; ②CaH2要密封保存.
【进行实验】
该小组同学设计的制取装置如图所示(固定装置略).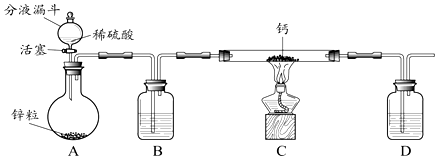
回答下列问题:
(1)写出Ca常温遇水发生反应的化学方程式: .
(2)B、D中所盛试剂相同,该试剂为(填名称);D中该试剂的作用是 .
(3)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是: .
【实验反思】
该小组同学通过反思提出问题:上述制得的CaH2是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量为m g的CaH2样品,按图所示连接仪器(固定装置略).
步骤2:将Y形管倾斜,使A中的水全部进入B中,样品全部反应后,冷却至室温,读取量筒读数为V mL.
(4)若该实验条件下的气体摩尔体积为Vm L/mol,当V=mL时(用m、Vm表示),表明制得的CaH2样品是纯净的.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,则2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为( )
A.﹣488.3 kJ/mol
B.+488.3 kJ/mol
C.﹣191 kJ/mol
D.+191 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com