
 是一种有机烯醚,可以用烃A通过下列路线获得A$→_{①}^{Br_{2}/CCl}$B$→_{②}^{NaOH水溶液/△}$C$→_{③}^{浓H_{2}SO_{4}/△}$
是一种有机烯醚,可以用烃A通过下列路线获得A$→_{①}^{Br_{2}/CCl}$B$→_{②}^{NaOH水溶液/△}$C$→_{③}^{浓H_{2}SO_{4}/△}$
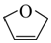 的同分异构体的结构简式(写出2种)HC≡CCH2CH2OH、CH3C≡CCH2OH
的同分异构体的结构简式(写出2种)HC≡CCH2CH2OH、CH3C≡CCH2OH分析 由合成流程可知,A与溴发生加成反应得B,B在碱性条件下水解得C,C在浓硫酸作用下发生脱水成醚,结合 的结构可逆推得到C为HOCH2CH=CHCH2OH,B为BrCH2CH=CHCH2Br,A为CH2=CHCH=CH2,以此来解答.
的结构可逆推得到C为HOCH2CH=CHCH2OH,B为BrCH2CH=CHCH2Br,A为CH2=CHCH=CH2,以此来解答.
解答 解:(1)A为CH2=CHCH=CH2,含有的官能团为碳碳双键,故答案为:碳碳双键;
(2)HOCH2CH=CHCH2OH发生取代反应生成 ,故答案为:取代反应;
,故答案为:取代反应;
(3)B为BrCH2CH=CHCH2Br,在氢氧化钠水溶液中发生取代反应生成HOCH2CH=CHCH2OH,方程式为BrCH2CH=CHCH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH=CHCH2OH+2NaBr,
故答案为:BrCH2CH=CHCH2Br+2NaOH$→_{△}^{H_{2}O}$HOCH2CH=CHCH2OH+2NaBr;
(4)有机醚  的同分异构体满足①链状结构;②能被CuO氧化成为醛类,说明分子中含有-CH2OH结构,且分子中含有C≡C或2个C=C键,可能的结构简式为HC≡CCH2CH2OH、CH3C≡CCH2OH,故答案为:HC≡CCH2CH2OH、CH3C≡CCH2OH.
的同分异构体满足①链状结构;②能被CuO氧化成为醛类,说明分子中含有-CH2OH结构,且分子中含有C≡C或2个C=C键,可能的结构简式为HC≡CCH2CH2OH、CH3C≡CCH2OH,故答案为:HC≡CCH2CH2OH、CH3C≡CCH2OH.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意逆合成法的应用,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①的平衡常数K1=$\frac{c(C{O}_{2})•c(Cu)}{c(CO)•c(CuO)}$ | |
| B. | 反应③的平衡常数K=$\frac{{K}_{1}}{{K}_{2}}$ | |
| C. | 对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值 | |
| D. | 对于反应③,恒温恒容下,增大压强,H2浓度一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 缩小体积加压 | B. | 使用催化剂 | C. | 增加A的浓度 | D. | 降温 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | A、B的单质与盐酸反应的速率:B>A | B. | B的氧化物具有两性 | ||
| C. | C和E在常温下可发生化学反应 | D. | A和E能形成共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子电子层数:A<B | |
| B. | 气态氢化物的稳定性:B<E | |
| C. | 氢化物的沸点:B<E | |
| D. | 若H2EO3的酸性弱于HClO4,则非金属性E<Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +CH3OH$?_{△}^{浓H_{2}SO_{4}}$
+CH3OH$?_{△}^{浓H_{2}SO_{4}}$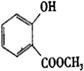 +H2O.反应类型是取代反应.
+H2O.反应类型是取代反应.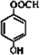 或
或 .
. )的合成路线(无机原料任选).
)的合成路线(无机原料任选). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1mol分枝酸最多可与3molNaOH发生中和反应 | |
| B. | 分子中含有2种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型不相同 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理不相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com