
 2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见表。下列说法正确的是
2NH3(g)+CO2(g) 在不同温度下,该反应平衡状态部分数据见表。下列说法正确的是 | 温度 | 平衡浓度/ (mol L-1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | | 0.1 |


科目:高中化学 来源:不详 题型:单选题
 Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )| A.60 s时Z的平衡浓度为O.03mol/L |
| B.将容器容积变为20 L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.若温度和体积不变,往容器内增加1 mol Y,Y的转化率将增大 |
| D.若升高温度,X的体积分数增大,则正反应的△H>O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
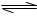 H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
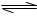 2HI(g)的平衡常数K的值为 。
2HI(g)的平衡常数K的值为 。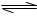 H2(g)+I2(g)的平衡常数,可采取的措施是 (选填字母)。
H2(g)+I2(g)的平衡常数,可采取的措施是 (选填字母)。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
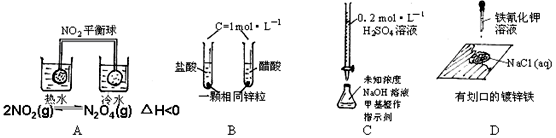
| 序号 | 实验现象 | 结 论 |
| A | 热水中平衡球颜色比冷水中深 | 升温,化学平衡向吸热反应方向移动 |
| B | 起始时产生气泡速率HCl > CH3COOH | 醋酸是弱电解质 |
| C | 溶液颜色由黄变橙,且30秒内不变色 | 已达滴定终点 |
| D | 划口处有蓝色沉淀 | 铁发生了析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pZ (g);ΔH<0,达化学平衡后,改变条件,下列表述不正确的是
pZ (g);ΔH<0,达化学平衡后,改变条件,下列表述不正确的是| A.增大压强,化学平衡不一定发生移动 |
| B.通入氦气,化学平衡不一定发生移动 |
| C.增加X或Y的物质的量,化学平衡一定发生移动 |
| D.其它条件不变,升高温度,化学平衡一定发生移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 WI2(g),当I2的转化率为20%时,达化学平衡状态。
WI2(g),当I2的转化率为20%时,达化学平衡状态。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 FeO(s)+CO(g)△H=akJ·mol—1,平衡常数为K;反应②CO(g)+1/2O2(g)=CO2(g) △H=bkJ·mol—1
FeO(s)+CO(g)△H=akJ·mol—1,平衡常数为K;反应②CO(g)+1/2O2(g)=CO2(g) △H=bkJ·mol—1| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
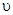 是速率、
是速率、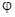 为混合物中CO含量,T为温度且T1>T2)
为混合物中CO含量,T为温度且T1>T2)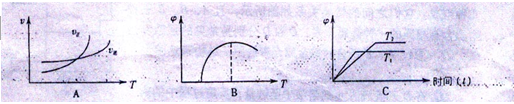
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com