
溴乙烷是有机合成的重要原料。农业上用作仓储谷物、仓库及房舍等的熏蒸杀虫剂;也常用于汽油的乙基化、冷冻剂和麻醉剂。实验室用NaBr、浓H2SO4、乙醇为原料,制备溴乙烷,反应的化学方程式为:
已知反应物的用量:0.3 mol NaBr(s);0.25 mol乙醇;36 mL浓硫酸(溶质质量分数为98%,密度为1.84 g/mL);25 mL水,其中乙醇的密度为0.80 g/mL。回答下列问题:
(1)该实验应选择下图中的 (填“a”或“b”)装置。
(2)冷凝管中的冷凝水的流向应是( )
A.A进B出 B.B进A出 C.从A进或B进均可
(3)上述实验完成后,需要将烧瓶中的有机物蒸馏出来,所得馏出液中含有 。
(4)用棕黄色的粗溴乙烷制取无色的溴乙烷应加入的试剂是 ,必须使用的仪器是 。
(5)本实验的产率为60%,则可制取溴乙烷 g。
(6)为除去溴乙烷中残留的少量水,可选用无水CaCl2作干燥剂,并蒸馏。为证明最终得到的产品——溴乙烷中含有溴元素,可采取的实验方法是 。
【答案】
(1)a (2)B (3)CH3CH2Br CH3CH2OCH2CH3
(4)NaOH溶液;分液漏斗
(5)16.35g
(6)将卤代烃和氢氧化钠溶液混合共热,所的产物用硝酸酸化后,再加入硝酸银溶液后,若有浅黄色沉淀则证明含有溴元素。
【解析】
(1)根据反应条件选择加热的酒精灯。
(2)冷凝管中的冷凝水的流向应是从低处流向高处。
(3)主产物有溴乙烷,和乙醇加热发生取代反应的乙醚。
(4)用棕黄色的粗溴乙烷里含有液溴,除去溴用NaOH,出现分层,必须使用的仪器是分液漏斗。
(5)本实验的产率为60%,则可制取溴乙烷 g。
NaBr + CH3CH2OH + H2SO4-----NaHSO4 + CH3CH2Br + H2O
1 1 1 1 109 1
0.3mol 0.25mol 0.036*1.84*0.98/98 x
(6)为除去溴乙烷中残留的少量水,可选用无水CaCl2作干燥剂,并蒸馏。为证明最终得到的产品溴乙烷中含有溴元素,可采取的实验方法是将卤代烃和氢氧化钠溶液混合共热,所的产物用硝酸酸化后,再加入硝酸银溶液后,若有浅黄色沉淀则证明含有溴元素。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
用惰性电极电解下列溶液一小段时间后,加入一定量的另一种物质(括号内),溶液能与原来溶液完全一样的是 ( )
A.CuSO4[Cu(OH)2] B.NaOH(NaOH)
C.NaCl(NaCl) D.CuCl2(CuCl2)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A物质的分子结构简式如右:lmol A与足量NaOH溶液
混合共热,充分反应后最多消耗NaOH的物质的量为( )
A.6mol B.8mo1 C.7mol D.9mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃的结构简式为
Embed ChemDraw.Document.6.0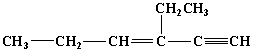 ,分子中含有四面体结构的碳原子数为a,在同一条直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别是( )
,分子中含有四面体结构的碳原子数为a,在同一条直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别是( )
A. 4、4、5 B. 2、5、4 C. 4、3、6 D. 4、6、4
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z- ,Y+和Z-离子具有相同的电子层结构。下列说法正确的是( )
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z- D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
〔化学—选修2:化学与技术〕(15分)
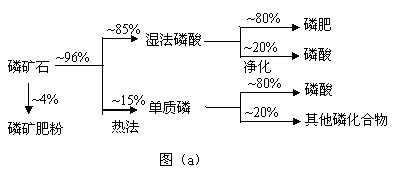
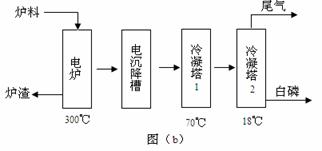
磷矿石主要以磷酸钙〔Ca3(PO4)2·H2O〕和磷灰石〔Ca3(OH)(PO4)3〕等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。

部分物质的相关性质如下:
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水,具有还原性 |
| SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 ℅。
(2)以磷灰石为原料,湿法磷酸过程中Ca3F(PO4)3反应的化学方程式为: 。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品磷酸 吨。
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是: (填化学式)冷凝塔1的主要沉积物是: 冷凝塔2的主要沉积物是:
(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去
再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
为实现下列 实验目的,依据下表提供的主要仪器,所用试剂合理的是
实验目的,依据下表提供的主要仪器,所用试剂合理的是
| 选项 | 实验目的 | 主要 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液,0.1000mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列金属冶炼的反应原理,错误的是( )
A.2NaCl(熔融) 2Na+Cl2↑ B.MgO+H2
2Na+Cl2↑ B.MgO+H2  Mg+H2O
Mg+H2O
C.Fe2O3+3CO 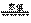 2Fe+3CO2 D.2HgO
2Fe+3CO2 D.2HgO  2Hg+O2↑
2Hg+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com