
分析 碳的质量分数是52.16%,氢的质量分数是13.14%,则氧元素质量分数是1-52.16%-13.14%=34.7%,则该物质中碳、氢、氧原子个数之比=$\frac{52.16%}{12}$:$\frac{13.14%}{1}$%:$\frac{34.7%}{16}$4.34%:13,14%:2.17%=2:6:1,以此来解答.
解答 解:碳的质量分数是52.16%,氢的质量分数是13.14%,则氧元素质量分数是1-52.16%-13.14%=34.7%,则该物质中碳、氢、氧原子个数之比=$\frac{52.16%}{12}$:$\frac{13.14%}{1}$%:$\frac{34.7%}{16}$4.34%:13,14%:2.17%=2:6:1,
(1)由原子个数比可知该有机物的实验式为C2H6O,
答:该有机物的实验式为C2H6O;
(2)设分子式为(C2H6O)n,则(12×2+6+16)×n=46,解得n=1,则分子式为C2H6O,
答:有机物的分子式为C2H6O.
点评 本题考查有机物分子式计算的确定,为高频考点,把握分子式、实验式的确定方法为解答的关键,侧重分析与计算能力的考查,注意原子个数比的计算,题目难度不大.


科目:高中化学 来源: 题型:解答题

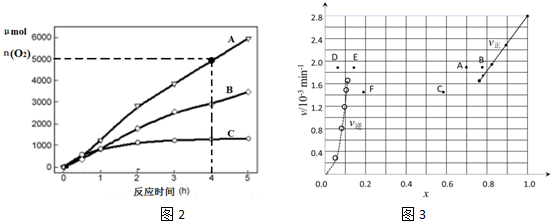
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
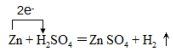 或
或 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com