
【题目】已知4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则正确的关系式为( )
4NO(g)+6H2O(g),若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则正确的关系式为( )
A. 4υ(NH3)=5υ(O2) B. 5υ(O2)=6υ(H2O)
C. 2υ(NH3)=3υ(H2O) D. 4υ(O2)=5υ(NO)
 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图______________。
(2)写出Y元素最高价氧化物分别与HCl、NaOH溶液反应的离子方程式____________________、______________________。
(3)写出Z的电子排布式_____、铬原子的简化的电子排布式______。
(4)元素T与氯元素相比,非金属性较强的是___(用元素符号表示),下列表述中能证明这一事实的是___(填字母代号)。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两单质在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___(填元素符号),理由是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:3A(g)![]() 3B(?)+C(?)(正反应是吸热反应),随着温度的升高,气体平均相对分子质量有减小趋势,则下列判断正确的是
3B(?)+C(?)(正反应是吸热反应),随着温度的升高,气体平均相对分子质量有减小趋势,则下列判断正确的是
A. B和C可能都是固体 B. B和C一定都是气体
C. 若C为固体,则B一定是气体 D. B和C不可能都是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列五种溶液:盐酸、NH3·H2O、NH4HSO4、NaOH、CH3COOH。回答下列问题:
(1)将1 L pH=2的HCl溶液分别与0.01 mol· L-1的NH3· H2O溶液x L、0.01 mol· L-1的NaOH溶液y L充分反应至中性,x、y大小关系为: y_____x(填“>”“<”或“=”)。
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是_____(填写序号)。
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的______曲线(填写序号)。
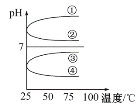
(4)室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加0.01 mol·L-1 NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+) ______2c(SO42- )(填“>”“=”或“<”);用NH4HSO4与氢氧化钡溶液制取硫酸钡,若溶液中SO42- 完全沉淀,则反应后溶液的pH______7(填“>”“=”或“<”),该反应的离子方程式为_______________。
(5)25 ℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是________________(用离子方程式表示)。向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将_______(填“正向”“不”或“逆向”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于古籍中的记载说法不正确的是
A. 《本草纲目》“烧酒”条目下写道自元时始创其法,用浓酒和糟入甑,蒸令气上其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏
B. 《吕氏春秋·别类编》中“金(即铜)柔锡柔,合两柔则刚” 体现了合金硬度方面的特性
C. 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了显色反应
D. 《抱朴子·金丹篇》中记载:“丹砂(HgS)烧之成水银,积变又成丹砂”,该过程发生了分解、化合、氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.02mol·L—1的HCN溶液与0.02mol·L—1的NaCN溶液等体积混合,已知混合溶液中C(CN-)<C(Na+),则下列关系中,正确的是:
A.C(Na+)>C(CN-)>C( H+)>C(OH-)
B.C(HCN)+C (CN-)=0.04mol·L-1
C.C(CN-)>C(HCN)
D.C(Na+)+C(H+)= C(CN-)+C(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态溴原子的价层电子轨道排布式为________。第四周期中,与溴原子未成对电子数相同的金属元素有_______种。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________(填标号)。
A.都属于p区主族元素B.电负性都比镁大
C.第一电离能都比镁大D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________;[AlCl4]-的立体构型名称为______。
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________。
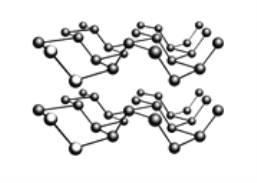
A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是_________。
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为______。
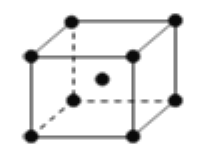
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酞,别名非诺夫他林,是制药工业原料,其结构如图所示,有关酚酞说法不正确的是

A. 分子式为C20H14O4
B. 可以发生取代反应、加成反应、氧化反应
C. 含有的官能团有羟基、酯基
D. 1mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值为10mol和4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,四种装置中所盛有的溶液体积均为200ml,浓度均为0.6mol/L,工作一段时间后,测得导线上均通过了0.2mol电子,此时溶液中的![]() 由大到小的顺序是
由大到小的顺序是
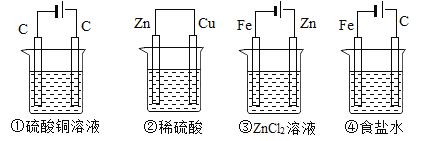
①硫酸铜溶液 ②稀硫酸 ③氯化锌溶液 ④食盐水
A. ④②①③ B. ④③①② C. ④③②① D. ①③②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com