
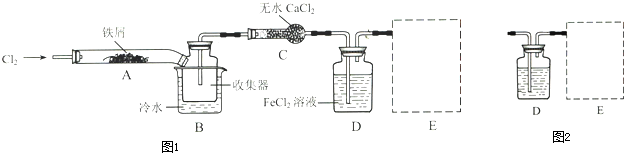
| ||
| ||
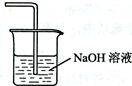 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
| A、CO2、SiO2都能与NaOH发生反应 |
| B、CO2和SiO2 都能与水反应 |
| C、CO2是酸性氧化物,SiO2是两性氧化物 |
| D、CO2和SiO2都是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、磁性氧化铁溶于稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| B、Na2S溶液呈碱性:S2-+2H2O?H2S+2OH- |
| C、向硝酸银溶液中逐滴滴入稀氨水至过量:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O |
| D、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
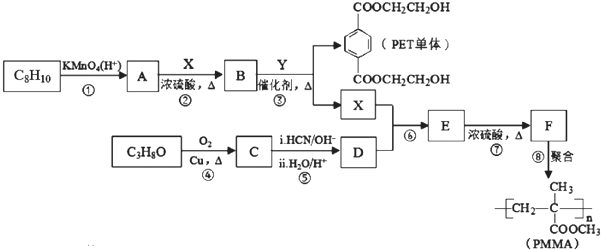
| 催化剂 |
| △ |
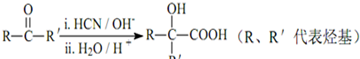
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH试纸放入溶液中,观察其颜色变化并与标准比色卡对照 |
| B、将溶液倒在pH试纸上,观察其颜色变化并与标准比色卡对照 |
| C、用干燥、洁净玻璃棒蘸取溶液,滴在pH试纸上,观察其颜色变化并与标准比色卡对照 |
| D、在试管内放入少量溶液并煮沸,把pH试纸放在管口观察其颜色并与标准比色卡对照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 80℃,通电 |
| Ⅰ |
| 室温,KCl |
| Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)25℃时,0.1mol?L-1的HA溶液中
(1)25℃时,0.1mol?L-1的HA溶液中| c(H+) |
| c(OH-) |
| c(H+) |
| c(HA) |
| c(HA) |
| A- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N | B、M | C、X | D、Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com