
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( ) 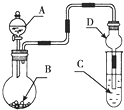
A.若A为浓盐酸,B为KMnO4晶体,C是紫色石蕊溶液,则C中溶液最终呈红色
B.若A为浓硫酸,B为Na2SO3固体,C中是NaOH溶液,实验仪器D可以起到防止溶液倒吸的作用
C.若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中溶液先产生白色沉淀后沉淀又溶解
D.若A为浓H2SO4 , B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊
【答案】B
【解析】解:A.若A为浓盐酸,B为KMnO4晶体,二者反应生成氯气,把氯气通到紫色石蕊溶液中,氯气与水反应生成HCl和HClO,HCl使紫色石蕊溶液变红,HClO具有漂白性,使溶液褪色,C中溶液最终呈无色,故A错误;
B.烧瓶中反应生成二氧化硫,二氧化硫与NaOH反应,C吸收尾气,D中球形干燥管中间部分较粗,盛放的液体的量较多,倒吸的液体靠自身重量回落,因此可以防止液体倒吸,故B正确;
C.若A为浓氨水,B为生石灰,滴入后反应生成氨气,氨气和铝离子反应生成氢氧化铝,但氢氧化铝不溶于氨水,所以C中产生白色沉淀不溶解,故C错误;
D.若A为浓硫酸,B为Cu,反应需要加热才能反应,如果不加热,则没有二氧化硫产生,所以C中溶液无变化,故D错误;
故选B.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】下列化学用语的表述正确的是( )
A.离子结构示意图 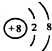 :可以表示16O2﹣ , 也可以表示18O2﹣
:可以表示16O2﹣ , 也可以表示18O2﹣
B.比例模型 ![]() :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
C.氯化铵的电子式为: ![]()
D.CO2的结构式为:O﹣C﹣O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以1,3﹣丁二烯,丙烯,乙炔等为原料合成 ![]() 流程图如图
流程图如图 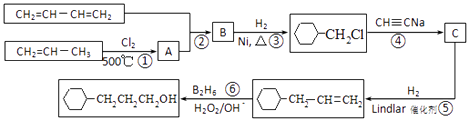
(1)反应①的反应类型是 , B中含有的官能团的名称 .
(2)写出反应②的化学方程式 .
(3)写出C的结构简式 .
(4)写出 ![]() 含有六元环且核磁共振氢谱有4组峰的同分异构体的结构简式 .
含有六元环且核磁共振氢谱有4组峰的同分异构体的结构简式 .
(5)根据以上合成信息,以乙烯为原料合成1,6﹣己二醇,其他试剂任选,写出合成的流程图 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种元素,A元素形成的﹣2价阴离子比氦原子的核外电子数多8个,B元素与A元素可组成一种化合物E,为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的金属元素,当2.4g C与足量热水反应时,在标准状况下放出气体2.24L,C形成正二价阳离子;D元素原子的M层上有7个电子.
(1)C在周期表中的位置 .
(2)D的气态氢化物与H2S、HF的稳定性由强到弱为(用化学式表示).
(3)写出淡黄色固体E的电子式 , 其中含有的化学键为 .
(4)钾元素与B元素位于同一主族,钾元素与A元素可形成K2A、K2A2、KA2等多种化合物,其中K2A2和KA2和CO2均可发生反应(反应与淡黄色固体E和CO2的反应类似),K2A2、KA2在医院、矿井、潜水、高空飞行中常用作供氧剂,为了维持气压稳定可以使用过氧化钾和超氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅酸盐的叙述中,正确的是 ( )
①硅酸盐大多都难溶于水 ②硅酸盐是构成地壳岩石的最主要成分
③硅酸盐中最常见的是Na2SiO3,它的水溶液俗称水玻璃
A. ③ B. ②③ C. ①② D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是一个化学过程的示意图. 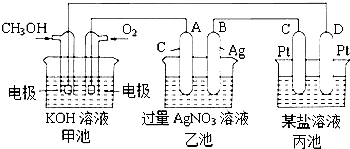
(1)图中乙池是装置.
(2)C(Pt)电极的名称是 .
(3)写出通入CH3OH的电极的电极反应式是 .
(4)乙池中反应的离子方程式为 .
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是
A.MgSO4 B.CuSO4 C.NaCl D.CuCl2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关试剂的保存方法,正确的是( )
A. 硝酸应该保存在无色的试剂瓶中
B. 新制的氯水通常保存在无色试剂瓶中
C. 氢氧化钠溶液保存在有玻璃塞的玻璃试剂瓶中
D. 氢氟酸保存在塑料瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可以采用热还原法制备金属镁(镁沸点为1107℃,熔点是648.8℃)。
(1)将碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]和焦炭按一定比例混合,放入真空管式炉中先升温至500℃保持一段时间,然后升温至1450℃反应制得镁。
①用碳还原法制备金属镁需要在真空中而不在空气中进行,其原因是。
②焦炭与碱式碳酸镁的物质的量的比值不同对镁的还原率有较大影响,结果如图。当比值大于15∶1时,还原率下降的原因可能是。
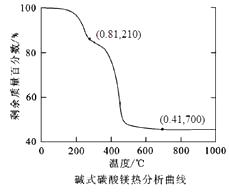
③碱式碳酸镁分解如图所示,写出在1450℃反应制得镁的化学反应方程式。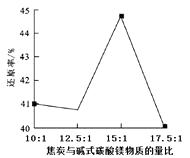
(2)工业上可以采用MgCl2溶液和Na2CO3溶液混合制备碱式碳酸镁,写出反应离子方程式。反应采用68℃,温度不宜高于68℃的原因是。
(3)工业采用电解MgCl2溶液产生Mg(OH)2 , 如图。然后用Mg(OH)2悬浊液吸收烟气中的二氧化碳,减少二氧化碳的排放同时产生碱式碳酸镁。该电池的阴极电极反应式为。电解时还得到副产物为。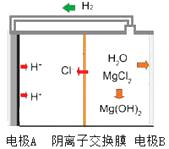
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.10gT2O含有的电子数为5NA
B.常温下,0.2L 0.5molL﹣1NH4NO3溶液的氮原子数小于0.2NA
C.用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NA
D.常温常压下,5.6gC2H4和C3H6的混合气体中含氢原子数为0.9NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com