
电解过程中放H2生碱型和放O2生酸型的实质是什么?在放H2生碱型的电解中,若滴入酚酞试液,哪一极附近溶液变红?
科目:高中化学 来源: 题型:
下列说法不正确的有( )
A.26 号元素铁属于d 区 B.主族族序数=其价电子数=最外层电子数
C.在周期表中,元素周期数=原子核外电子层数 D.最外层电子数=8的微粒都是稀有气体元素
查看答案和解析>>
科目:高中化学 来源: 题型:
已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和双原子分子M。(组成E分子的元素的原子序数都小于10,组成G分子的元素为第三周期的元素。)如下图,则下列判断中正确的是
A.常温常压下,L是一种液态有机物 B.E中化学键是极性键
C.G有漂白性 D.上述反应的类型是加成反应

查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于反应限度的叙述不正确的是
A.反应限度是一种平衡状态,此时反应已经停止
B.达到平衡状态时,正反应速率和逆反应速率相等
C.达到平衡状态时,反应物和生成物浓度都不再改变
D.达到平衡状态时,反应物的转化率已经最大
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种短周期元素,A元素的离子焰色反应为黄色。5.8 g B的氢氧化物恰好能与100 mL 2 mol·L—1盐酸完全反应;B原子核中质子数和中子数相等。F原子中无中子且F2在黄绿色气体C2中燃烧产生苍白色火焰。D元素原子的最外层电子数是次外层电子数的3倍;含E元素的化合物种类最多。根据上述条件回答:
(1)E的元素符号为 ,
(2)A、D形成淡黄色化合物A2D2,其电子式为 ,
(3)C2与ADF溶液反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求书写电极反应式和总方程式
(1)用惰性电极电解AgNO3溶液:
阳极反应式_______________________________________________________________;
阴极反应式_______________________________________________________________;
总反应离子方程式_________________________________________________________。
(2)用惰性电极电解MgCl2溶液
阳极反应式_______________________________________________________________;
阴极反应式_______________________________________________________________;
总反应离子方程式_________________________________________________________。
(3)用铁作电极电解NaCl溶液
阳极反应式_______________________________________________________________;
阴极反应式_______________________________________________________________;
总化学方程式_____________________________________________________________。
(4)用铜作电极电解盐酸溶液
阳极反应式_______________________________________________________________;
阴极反应式_______________________________________________________________;
总反应离子方程式_________________________________________________________。
(5)用Al作电极电解NaOH溶液
阴极反应式_______________________________________________________________;
阳极反应式_______________________________________________________________;
总反应离子方程式_________________________________________________________。
(6)用惰性电极电解熔融MgCl2
阴极反应式_______________________________________________________________;
阳极反应式_______________________________________________________________;
总反应离子方程式________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如下,下列说法不正确的是 ( )
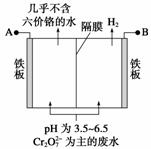
A.A为电源正极
B.阳极区溶液中发生的氧化还原反应为
Cr2O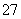 +6Fe2++14H+===2Cr3++6Fe3+
+6Fe2++14H+===2Cr3++6Fe3+ +7H2O
+7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O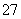 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)= ==2PbSO4(s)+2H2O(l)
==2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O电解,Al2O3+3H2↑
电解过程中,以下判断正确的是 ( )
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3 mol Pb | 生成2 mol Al2O3 |
| C | 正极:PbO2+4H++2e-===Pb2++2H2O | 阳极:2Al+3H2O-6e-===Al2O3+6H+ |
| D |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
溴乙烷是有机合成的重要原料。农业上用作仓储谷物、仓库及房舍等的熏蒸杀虫剂;也常用于汽油的乙基化、冷冻剂和麻醉剂。实验室用NaBr、浓H2SO4、乙醇为原料,制备溴乙烷,反应的化学方程式为:
已知反应物的用量:0.3 mol NaBr(s);0.25 mol乙醇;36 mL浓硫酸(溶质质量分数为98%,密度为1.84 g/mL);25 mL水,其中乙醇的密度为0.80 g/mL。回答下列问题:
(1)该实验应选择下图中的 (填“a”或“b”)装置。
(2)冷凝管中的冷凝水的流向应是( )
A.A进B出 B.B进A出 C.从A进或B进均可
(3)上述实验完成后,需要将烧瓶中的有机物蒸馏出来,所得馏出液中含有 。
(4)用棕黄色的粗溴乙烷制取无色的溴乙烷应加入的试剂是 ,必须使用的仪器是 。
(5)本实验的产率为60%,则可制取溴乙烷 g。
(6)为除去溴乙烷中残留的少量水,可选用无水CaCl2作干燥剂,并蒸馏。为证明最终得到的产品——溴乙烷中含有溴元素,可采取的实验方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com