


科目:高中化学 来源: 题型:
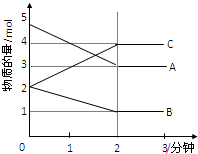 某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A,B,C均为气体).
某可逆反应在某体积为5L的密闭容器中进行,在从0-3分钟各物质的量的变化情况如图所示(A,B,C均为气体).查看答案和解析>>
科目:高中化学 来源: 题型:
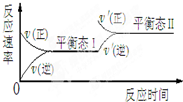 随着人类对温室效应和资源短缺等问题的重视,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前有一种方法是用CO2来生产燃料甲醇CH3OH.在体积不变的5L密闭容器中,充入一定量的CO2和 H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应)经过10min反应达到平衡,测得物质的浓度如下表所示.
随着人类对温室效应和资源短缺等问题的重视,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前有一种方法是用CO2来生产燃料甲醇CH3OH.在体积不变的5L密闭容器中,充入一定量的CO2和 H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应)经过10min反应达到平衡,测得物质的浓度如下表所示.| 物 质 | CO2 | H2 | CH3OH(g) | H2O(g) |
| 起始浓度(mol/L) | 1.0 | 3.0 | 0 | 0 |
| 10min末浓度(mol/L) | 0.75 | 0.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 用途或现象 | 体现浓硫酸的性质 |
| (1)浓硫酸使蓝矾变成白色 | |
| (2)浓硫酸使木条变黑 | |
| (3)浓硫酸与铜片共热 | |
| (4)浓硫酸的木炭共热产生气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
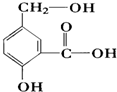 在某有机物A的分子其结构简式如图,请回答.
在某有机物A的分子其结构简式如图,请回答.查看答案和解析>>
科目:高中化学 来源: 题型:
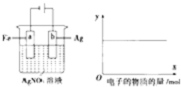 按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )| A、①③ | B、③④ |
| C、①②④ | D、①②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com