
| A.18.4 mol·L-1 | B.20.4 mol·L-1 | C.37.7% | D.38.5% |
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
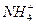 和H3O+、
和H3O+、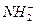 和OH-、N3-和O2-从某些性质来看,每组中的物质两两相似。据此推断,下列反应正确的是( )
和OH-、N3-和O2-从某些性质来看,每组中的物质两两相似。据此推断,下列反应正确的是( )A.Cu+2NH3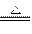 Cu(NH2)2+H2↑ Cu(NH2)2+H2↑ |
| B.CaO+2NH4Cl====CaCl2+2NH3↑+H2O |
C.3Mg(NH2)2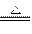 Mg3N2+4NH3↑ Mg3N2+4NH3↑ |
| D.NaCl+2NH3====NH4Cl+NaNH2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ρ1>ρ2>ρ3>ρ4 | B.ρ4>ρ3>ρ2>ρ1 |
| C.ρ2>ρ1>ρ4>ρ3 | D.ρ3>ρ4>ρ2>ρ1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
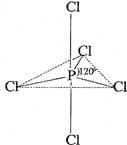
 反应所消耗的氧气在标准状况下的体积为 L。
反应所消耗的氧气在标准状况下的体积为 L。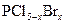 (
(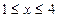 ,且x为整数)。
,且x为整数)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第四周期IVA族 | B.第五周期IVA族 |
| C.第四周期VA族 | D.第五周期VA族 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.气体B可能是O2,也可能是NO |
| B.固体粉末的组成为n(KNO3):n(Cu(NO3)2):n(AgNO3)=1:1:3 |
| C.固体粉末的组成为n(KNO3):n(Cu(NO3)2):n(AgNO3)=1:1:1 |
| D.气体A 中NO2与O2的体积比为9:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com