
 )与P(
)与P( ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )| A. | 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3:1 | |
| B. | 二者在NaOH醇溶液中均可发生消去反应 | |
| C. | 一定条件下,二者在NaOH溶液中均可发生取代反应 | |
| D. | Q的一氯代物只有1种,P的一溴代物有2种 |
分析 A.由结构对称性可知,均含2种H,但H原子数目不同;
B.Q中-Br与苯环相连不能发生消去反应,P中与-Cl相连C的邻位C上没有H;
C.卤代烃、甲基等均可发生取代反应;
D.Q、P中均含2种H.
解答 解:A.二者的核磁共振氢谱中均只出现两种峰,且峰面积之比分别为3:1、3:2,故A错误;
B.二者在NaOH醇溶液中均不能发生消去反应,故B错误;
C.卤代烃、甲基等均可发生取代反应,则一定条件下,二者在NaOH溶液中均可发生取代反应,故C正确;
D.Q、P中均含2种H,则一氯代物均有2种,故D错误;
故选C.
点评 本题考查有机物的结构与性质及推断,为高频考点,把握官能团与性质的关系为解答的关键,侧重结构对称性分析及卤代烃性质的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
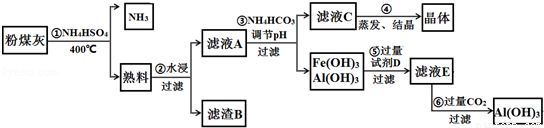
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
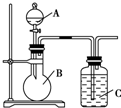 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
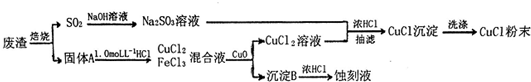
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-2-丁烯 | B. | 2,3-二甲基-1-丙烯 | ||
| C. | 3-甲基-1-丁烯 | D. | 2-甲基-1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
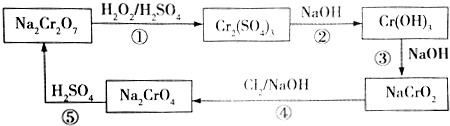
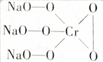 ,则Cr的化合价为+5,其中含有的化学键有离子键、共价键.
,则Cr的化合价为+5,其中含有的化学键有离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有离子键的化合物必是离子化合物 | |
| B. | 含有共价键的化合物就是共价化合物 | |
| C. | 共价化合物可能含离子键 | |
| D. | 离子化合物中一定含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
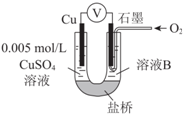 某小组同学利用原电池装置探究物质的性质.
某小组同学利用原电池装置探究物质的性质.| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
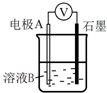 | Ⅰ | Fe | pH=2的 H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com