
分析 (1)在放电条件下,氮气跟氧气能直接化合生成无色的一氧化氮气体;一氧化氮不溶于水,在常温下易跟空气中的氧气化合,生成红棕色的二氧化氮气体;二氧化氮易溶于水,它溶于水后生成硝酸和一氧化氮,据此分析解答;
(2)硫磺、硝酸钾和木炭按一定比例混合,爆炸时会产生K2S、N2、CO2,根据氧化还原反应配平方程式,氧化剂中元素化合价降低,氧化产物是化合价升高后的产物,据此分析.
解答 解:(1)“雷雨发庄稼”,空气中的N2在放电条件下与O2直接化合生成无色且不溶于水的一氧化氮气体,N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;
一氧化氮的密度比空气略大,不稳定,常温下就易与空气中的O2反应生成红棕色的二氧化氮气体,2NO+O2=2NO2;
二氧化氮气体有毒,易与水反应生成硝酸(HN03)和一氧化氮,3NO2+H2O=2HNO3+NO;
生成的硝酸随雨水淋洒到大地上,同土壤中的矿物相互作用,生成可溶于水的硝酸盐可作氮肥,植物生长得更好,
故答案为:N2+O2 $\frac{\underline{\;放电\;}}{\;}$2NO、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO;
(2)硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时会产生K2S、N2、CO2,反应的方程式为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应物中有S、N元素的化合价降低,则硫、硝酸钾是氧化剂,C的化合价从0价升高到+4价,则二氧化碳是氧化产物,化学方程式中氧化剂KNO3,S,还原剂C,2molKNO3完全反应电子转移12mol,
结合电子守恒得到:2KNO3~N2~10e-,3C~12e-,
12KNO3~6N2~15C~15CO2~60e-,
12 15
0.3mol 0.375mol
0.3mol硝酸钾完全反应时,被它氧化的碳质量=0.375mol×12g/mol=4.5g,
故答案为:S+2KNO3+3C=K2S+N2↑+3CO2↑;4.5.
点评 本题考查了化学方程式书写、氧化还原反应电子转移守恒的计算,注意知识的积累,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 甲同学准确称取5.0gNaCl配制一定物质的量浓度的溶液时,乙同学发现NaCl固体与砝码放反了,但乙同学认为这个错误操作对实验结果没有影响 | |
| B. | 做酯化反应反应混合液的配制应先加乙醇,再加浓硫酸,冷却后最后加入乙酸 | |
| C. | 洗涤沉淀的方法是直接向过滤器中加入适量蒸馏水,然后让水自然流下 | |
| D. | 要检验滴有稀硫酸的蔗糖溶液是否水解,可加入银氨溶液,再水浴加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 城市 | 北京 | 上海 | 天津 | 重庆 | 南京 | 厦门 | 珠海 | 汕头 | 济南 | 杭州 | 成都 |
| 污染指数 | 92 | 72 | 82 | 98 | 95 | 25 | 47 | 54 | 76 | 67 | 87 |
| 首要污染物 | TSP | NOx | TSP | SO2 | TSP | TSP | TSP | TSP | |||
| 空气级别 | Ⅱ | Ⅱ | Ⅱ | Ⅱ | Ⅱ | Ⅰ | Ⅰ | Ⅱ | Ⅱ | Ⅱ | Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4是含氢质量分数最高的有机物 | |
| B. | CH4、CO、H2O均属于共价化合物 | |
| C. | 实验室可用排水法收集CH4、CO、N2 | |
| D. | CO可用HCOOH制取,说明CO是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


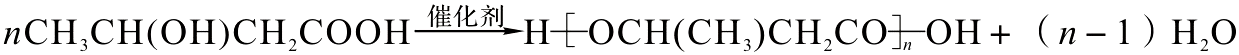 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com