
| A. | c(OH-)=c(R+)=0.01mol•L-1 | B. | c(R+)>c(H+) | ||
| C. | c(ROH)<c(R+) | D. | c(ROH)<c(OH-) |
分析 常温下,0.1mol•L-1 ROH溶液的pH=12,溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$=10-2mol/L,说明此碱为一元弱碱,溶液中存在电离平衡,结合溶液中电离分析离子浓度大小.
解答 解:常温下,0.1mol•L-1 ROH溶液的pH=12,溶液中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-12}}$=10-2mol/L,说明此碱为一元弱碱,溶液中c(OH-)>c(H+),溶液中存在电离平衡,ROH?R-+OH-,H2O?H++OH-,(OH-)>c(R+)=0.01mol•L-1 ,依据电离平衡可知c(ROH)>c(R+),c(ROH)>c(OH-),所以溶液中存在的离子浓度大小为c(R+)>c(H+),故选B.
点评 本题考查了弱电解质电离平衡的分析判断,注意溶液中存在水的电离平衡,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中和盐酸:CO${\;}_{{3}_{\;}}$2-+2H+=H2O+CO2↑ | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O | |
| C. | 向碳酸氢铵溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 用MnS除去MnCl2溶液中的Cu2+:MnS+Cu2+=CuS+Mn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c mol/L | B. | 3c mol/L | C. | $\frac{3c{V}_{1}}{{V}_{2}}$mol/L | D. | $\frac{c{V}_{1}}{{V}_{2}}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳分子的电子式: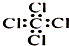 | B. | 对硝基甲苯的结构简式: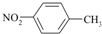 | ||
| C. | 羟基的电子式: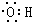 | D. | 乙醛的结构简式:CH3COH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
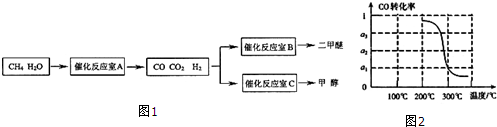
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com