
| A、饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+3H+ |
| B、向Ca(HCO3)2中加入少量Ca(OH)2:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| C、苯酚钠溶液通入足量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| D、乙醛和银氨溶液反应:CH3CHO+2Ag(NH3)2++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O |
| ||


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、棉花、羊毛、蚕丝均属于天然纤维素 |
| B、石油的分馏和裂化均属于化学变化 |
| C、油脂都不能使溴的四氯化碳溶液褪色 |
| D、甲烷、乙醇、乙酸在一定条件下都能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
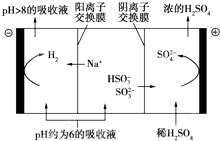 最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.| n(SO32-):n(HSO3- ) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯水通过SO2后溶液的酸性增强 |
| B、向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀 |
| C、Na、Fe等金属在一定条件下与水反应都生成H2和对应的碱 |
| D、浓硫酸、浓硝酸在加热条件下能将木炭氧化为二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com