
ŌŚĖįŠŌĢõ¼žĻĀ£¬“ĪĀČĖįÄĘ”¢¹żŃõ»ÆĒā¶¼ÓŠŗÜĒæµÄŃõ»ÆŠŌ£¬æɽ«Fe2+Ńõ»ÆĪŖFe3+£®Mg(OH)2ŗĶFe(OH)2ŌŚČÜŅŗÖŠÉś³ÉŹ±³Ź½ŗדĪļ»ņŠõדĪļ³Įµķ£¬¶ųMgCO3ŌŚĖ®ÖŠÖó·ŠæÉ×Ŗ±äĪŖMg(OH)2£®”°Ā±æé”±µÄÖ÷ŅŖ³É·ÖĪŖMgCl2(ŗ¬ÓŠFeCl2”¢FeCl3”¢MnCl2µČŌÓÖŹ)£®ČōŅŌĖüĪŖŌĮĻ£¬°“ĻĀĶ¼¹¤ŅÕĮ÷³ĢæÉÖʵƔ°ĒįÖŹŃõ»ÆĆ¾”±£®ŅŖĒó²śĘ·²»ŗ¬ŌÓÖŹĄė×Ó£¬¶ųĒŅ³É±¾½ĻµĶ£¬Į÷³ĢÖŠČÜŅŗpHµ÷½ŚŗĶĖłÓĆŹŌ¼ĮæɲĪæ¼±ķ1”¢±ķ2Ą“Č·¶Ø£®


ĒėĢīĻĀĮŠæÕ°×£ŗ
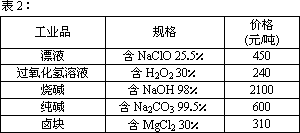
(1)ŌŚ²½Öč¢ŚÖŠ¼ÓČėĪļÖŹX£¬×ī¼ŃµÄŃ”ŌńÓ¦ŹĒ________£¬ĄķÓÉŹĒ________£»²½Öč¢ŚÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________£®
(2)ŌŚ²½Öč¢ŪÖŠŅŖæŲÖĘpH£½9.8£¬ĘäÄæµÄŹĒ________£®
(3)ŌŚ²½Öč¢ÜÖŠ¼ÓČėĪļÖŹÓ¦ŹĒ________£®
(4)ŌŚ²½Öč¢ŻÖŠ·¢ÉśµÄ»Æѧ·½³ĢŹ½ĪŖ________£®
 ŌĘÄĻŹ¦“óø½Š”Ņ»ĻßĆūŹ¦ĢįÓÅ×÷ŅµĻµĮŠ“š°ø
ŌĘÄĻŹ¦“óø½Š”Ņ»ĻßĆūŹ¦ĢįÓÅ×÷ŅµĻµĮŠ“š°ø ³å“Ģ100·Öµ„ŌŖÓÅ»ÆĮ·æ¼¾ķĻµĮŠ“š°ø
³å“Ģ100·Öµ„ŌŖÓÅ»ÆĮ·æ¼¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ŠÅĻ¢æØ ³£ĪĀĻĀĢ¼ĖįøĘÄŃČÜÓŚĖ®£¬ĒāŃõ»ÆøĘĪ¢ČÜÓŚĖ®£¬ĀČ»ÆøĘŅ×ČÜÓŚĖ®£®“ĪĀČĖįøĘŅ×ČÜÓŚĖ®£¬ĖįŠŌĢõ¼žĻĀ²»ĪČ¶Ø”¢100”ćCŹ±·¢Éś·Ö½ā·“Ó¦£® 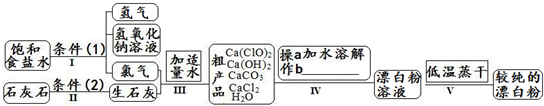 £Ø1£©Į÷³ĢI µĆµ½ÅضČĪŖ80g?L-1ĒāŃõ»ÆÄĘČÜŅŗ£¬ĘäĪļÖŹµÄĮæÅØ¶ČŹĒ 2 2 mol?L-1£®£Ø2£©Š“³öĮ÷³ĢI·¢Éś·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½£¬²¢ÓĆĖ«ĻßĒűķŹ¾Ęäµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ£ŗ   øßĪĀ øßĪĀ £®£Ø3£©Į÷³ĢIIIÖŠ·¢ÉśĮ½øö·“Ó¦£¬Š“³öĘäÖŠµÄŃõ»Æ»¹Ō·“Ó¦µÄ»Æѧ·“Ó¦·½³Ģ 2Cl2+2Ca£ØOH£©2ØTCa£ØClO£©2+CaCl2+2H2O 2Cl2+2Ca£ØOH£©2ØTCa£ØClO£©2+CaCl2+2H2O £®ĘäÖŠŃõ»Æ¼ĮŹĒCl2 Cl2 £»»¹Ō¼ĮŹĒCl2 Cl2 £®£ØŠ“»ÆѧŹ½£©£Ø4£©Į÷³ĢIVÖŠ²Ł×÷bŹĒ£ŗ ¹żĀĖ ¹żĀĖ £®£ØŠ“Ćū³Ę£©£Ø5£©Į÷³ĢV½ųŠŠµĶĪĀÕōøɵÄŌŅņŹĒ£ŗ Ca£ØClO£©2ŌŚ100”ćCŹ±·¢Éś·Ö½ā·“Ó¦ Ca£ØClO£©2ŌŚ100”ćCŹ±·¢Éś·Ö½ā·“Ó¦ £®£Ø6£©ÓĆ»Æѧ·½³ĢŹ½ĖµĆ÷½Ļ“æµÄ“ĪĀČĖįøĘ·ŪÄ©±ŲŠėĆÜ·ā±£“ęµÄŌŅņ Ca£ØClO£©2+CO2+H2OØTCaCO3+2HClO Ca£ØClO£©2+CO2+H2OØTCaCO3+2HClO £®£Ø7£©ĀČĖ®ŗĶ“ĪĀČĖįøʶ¼ÄÜĘšĘÆ°×”¢Ļū¶¾×÷ÓĆ£®ŹĒŅņĪŖĖüĆĒ¶¼ÄܲśÉśĶ¬Ņ»ÖÖĪļÖŹ£¬Š“³öĀČĘųÓėĖ®·“Ó¦²śÉśøĆĪļÖŹµÄ»Æѧ·½³ĢŹ½ Cl2+H2O  HCl+HClO HCl+HClOCl2+H2O £® HCl+HClO HCl+HClO£Ø8£©ŌŚĖįŠŌĢõ¼žĻĀ“ĪĀČĖįøʵÄŃõ»ÆŠŌ±ČĀČĘųĒ棬Äܽ«äåĄė×ÓŃõ»Æ³Éäåµ„ÖŹ£¬¶ų“ĪĀČĖįøĘÖŠµÄĀČŌŖĖŲŌņ±»»¹ŌĪŖøŗŅ»¼ŪµÄĀČĄė×Ó£¬ŃõŌŖĖŲŌņ×Ŗ»ÆĪŖĖ®£®ŹŌŠ“³ö“ĪĀČĖįøĘŗĶĻ”ŃĪĖįµÄ»ģŗĻĪļÓėäå»ÆÄĘ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ Ca£ØClO£©2+4HCl+4NaBr=CaCl2+4NaCl+2Br2+2H2O Ca£ØClO£©2+4HCl+4NaBr=CaCl2+4NaCl+2Br2+2H2O £®
²éæ““š°øŗĶ½āĪö>> æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā ”¾»Æѧ--Ń”ŠŽ2£ŗ»ÆѧÓė¼¼Źõ”æ×ŌĄ“Ė®Éś²śµÄĮ÷³ĢŹ¾ŅāĶ¼¼ūĻĀ£ŗ  £Ø1£©»ģÄż¼Į³żČ„Šüø”ĪļÖŹµÄ¹ż³Ģ ¢Ū ¢Ū £ØĢīŠ“ŠņŗÅ£©¢ŁÖ»ŹĒĪļĄķ±ä»Æ ¢ŚÖ»ŹĒ»Æѧ±ä»Æ ¢ŪŹĒĪļĄķŗĶ»Æѧ±ä»Æ FeSO4?7H2OŹĒ³£ÓƵĻģÄż¼Į£¬ĖüŌŚĖ®ÖŠ×īÖÕÉś³É Fe£ØOH£©3 Fe£ØOH£©3 ³Įµķ£®£Ø2£©ČōŅŖ³żČ„Ca2+”¢Mg2+æÉŅŌĶłĖ®ÖŠ¼ÓČėŹÆ»ŅŗĶ“æ¼ī£¬ŹŌ¼ĮĢī¼ÓŹ±ĻČ¼Ó ŹÆ»Ņ ŹÆ»Ņ ŗó¼Ó“æ¼ī “æ¼ī £¬ŌŅņŹĒ¹żĮæµÄøĘĄė×ÓæÉĶعż“æ¼īŹ¹Ö®³ĮµķĻĀĄ“ ¹żĮæµÄøĘĄė×ÓæÉĶعż“æ¼īŹ¹Ö®³ĮµķĻĀĄ“ £®£Ø3£©ĀČĘųĻū¶¾£¬ŹĒŅņĪŖĖüÓėĖ®·“Ӧɜ³ÉĮĖHClO£¬“ĪĀČĖįµÄĒæŃõ»ÆŠŌÄÜɱĖĄĖ®ÖŠµÄ²”¾ś£Ø²»ÄÜÖ±½ÓÓĆ“ĪĀČĖįĪŖ×ŌĄ“Ė®Ļū¶¾ŹĒŅņĪŖ“ĪĀČĖįŅ×·Ö½ā£¬ĒŅ¶¾ŠŌ½Ļ“󣩣® Cl2+H2O?HCl+HClO K=4.5”Į10-4 Ź¹ÓĆĀČĘųĪŖ×ŌĄ“Ė®Ļū¶¾æÉŅŌÓŠŠ§µŲæŲÖĘ“ĪĀČĖįµÄÅØ¶Č£¬Ēė½įŗĻĘ½ŗā³£Źż½āŹĶŌŅņ£ŗ ÓÉĀČĘųÓėĖ®·“Ó¦µÄĘ½ŗā³£ŹżæÉÖŖ£¬øĆ·“Ó¦µÄĻŽ¶ČŗÜŠ”£¬Éś³ÉµÄHClOÅضČŗÜŠ”£¬ĒŅĖę×ÅHClOµÄĻūŗÄ£¬Ę½ŗā»į²»¶ĻĻņÕż·“Ó¦ŅĘ¶Æ£¬²¹³äHClO ÓÉĀČĘųÓėĖ®·“Ó¦µÄĘ½ŗā³£ŹżæÉÖŖ£¬øĆ·“Ó¦µÄĻŽ¶ČŗÜŠ”£¬Éś³ÉµÄHClOÅضČŗÜŠ”£¬ĒŅĖę×ÅHClOµÄĻūŗÄ£¬Ę½ŗā»į²»¶ĻĻņÕż·“Ó¦ŅĘ¶Æ£¬²¹³äHClO £®ĻĀĮŠĪļÖŹÖŠ£¬¢Ł¢Ū ¢Ł¢Ū æÉŅŌ×÷ĪŖĀČĘųµÄ“śÓĆĘ·£ØĢīŠ“ŠņŗÅ£©£®¢Ł³ōŃõ ¢ŚNH3£ØŅŗ£© ¢ŪK2FeO4 ¢ÜSO2 £Ø4£©ÓŠŠ©µŲĒųµÄĢģČ»Ė®ÖŠŗ¬ÓŠ½Ļ¶ąµÄøĘ”¢Ć¾Ąė×Ó£®ÓĆĄė×Ó½»»»Ź÷Ö¬Čķ»ÆÓ²Ė®Ź±£¬ĻČŗó°ŃĖ®Ķعż·Ö±š×°ÓŠ Ńō Ńō Ąė×Ó½»»»Ź÷Ö¬ŗĶŅõ Ņõ Ąė×Ó½»»»Ź÷Ö¬µÄĄė×Ó½»»»Öł£ØĢī”°Ņõ”±»ņ”°Ńō”±£¬ŃōĄė×Ó½»»»Ź÷Ö¬ĪŖHRŠĶ£¬ŅõĄė×Ó½»»»Ź÷Ö¬ĪŖR”äOHŠĶ£©£®£Ø5£©²ā¶ØĖ®ÖŠµÄČܽāŃõ£ŗĮæČ”40mLĖ®Ńł£¬ŃøĖŁ¼ÓČėMnSO4ŗĶKOH»ģŗĻČÜŅŗ£¬ŌŁ¼ÓČėKIČÜŅŗ£¬Į¢¼“ČūŗĆČū×Ó£¬Õńµ“Ź¹ĶźČ«·“Ó¦£®“ņæŖČū×Ó£¬ŃøĖŁ¼ÓČėŹŹĮæĮņĖįČÜŅŗ£¬“ĖŹ±ÓŠµāµ„ÖŹÉś³É£®ÓĆ0.010mol/LNa2S2O3ČÜŅŗµĪ¶ØÉś³ÉµÄµā£¬ĻūŗÄĮĖ6.00mL Na2S2O3ČÜŅŗ£®ŅŃÖŖŌŚ¼īŠŌČÜŅŗÖŠ£¬ŃõĘųÄÜŃøĖŁŃõ»ÆMn2+£¬Éś³ÉĪļŌŚĖįŠŌĢõ¼žĻĀæÉŅŌ½«µāĄė×ÓŃõ»ÆĪŖµāµ„ÖŹ£¬±¾ÉķÖŲŠĀ»¹ŌĪŖMn2+£®ÉĻŹö¹ż³Ģ·¢ÉśµÄ·“Ó¦æɱķŹ¾ĪŖ£ŗ2Mn2++4OH-+O2=2MnO£ØOH£©2 MnO£ØOH£©2+2I-+4H+=I2+Mn2++3H2O I2+2S2O32-=2I-+S4O62- ŌņĖ®ÖŠµÄČܽāŃõĮæĪŖ 12.0 12.0 mg?L-1£®²éæ““š°øŗĶ½āĪö>> æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ £Ø10·Ö£©µāĖį¼ŲŹĒŅ»ÖÖ°×É«½į¾§·ŪÄ©£¬ĪŽ³ōĪŽĪ¶”£ŌŚĖįŠŌĢõ¼žĻĀµāĖį¼ŲŹĒŅ»ÖÖ½ĻĒæµÄŃõ»Æ¼Į£¬ÓėĒāµāĖį”¢¶žŃõ»ÆĮņµČ»¹ŌŠŌĪļÖŹ×÷ÓĆ£¬±»»¹ŌĪŖµ„ÖŹµā£¬ŌŚ¼īŠŌ½éÖŹÖŠ£¬µāĖį¼ŲÄܱ»ĀČĘų”¢“ĪĀČĖįŃĪµČŃõ»ÆĪŖøßµāĖį¼Ų”£µāĖį¼ŲŌŚ³£ĪĀĻĀĪČ¶Ø£¬¼ÓČČÖĮ560 ”ęæŖŹ¼·Ö½ā”£¹¤ŅµÉś²śµāĖį¼ŲµÄĮ÷³ĢČēĻĀĶ¼ĖłŹ¾”£ £Ø1£©ŌŚ·“Ó¦Ę÷ÖŠ·¢ÉśµÄ·“Ó¦I2£«KClO3£«H2O”śKH(IO3)2£«KCl£«Cl2£ØĪ“ÅäĘ½£©£¬Éś³ÉĮ½ÖÖ»¹Ō²śĪļĖłµĆµē×ÓŹżÄæĻąĶ¬£¬ĒėŠ“³öŅŃÅäĘ½µÄøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ”£ £Ø2£©²½Öč¢ŚÖŠ£¬ÓĆĻõĖį¶ų²»ÓĆHI£¬ĘäŌŅņæÉÄÜŹĒ ”£ £Ø3£©²½Öč¢ŪŅŖ±£³ÖČÜŅŗĪ¢·Š1Š”Ź±ŅŌĶźČ«ÅųöĀČĘų£¬ÅųöĀČĘųµÄŌŅņĪŖ ”£ £Ø4£©²ĪÕÕĻĀ±ķµāĖį¼ŲµÄČܽā¶Č£¬²½Öč¢ĻµĆµ½µāĖį¼Ų¾§Ģ壬Ӧ²ÉÓƵķ½·ØŹĒ ”£
£Ø5£©KIO3æÉÓƵē½āµÄ·½·ØÖĘµĆ£¬ŌĄķŹĒŅŌŹÆÄ«ĪŖŃō¼«£¬ŅŌ²»ŠāøÖĪŖŅõ¼«£¬ŌŚŅ»¶ØĪĀ¶ČŗĶµēĮ÷ĻĀµē½āKIČÜŅŗ”£×Ü·“Ó¦·½³ĢŹ½ĪŖKI£«3H2O=KIO3£«3H2”ü£¬ŌņŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>> æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012½ģ±±¾©ŹŠĖ³ŅåĒųøßČż¼ā×ÓÉś×ŪŗĻĖŲÖŹÕ¹Ź¾»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŹµŃéĢā £Ø10·Ö£©µāĖį¼ŲŹĒŅ»ÖÖ°×É«½į¾§·ŪÄ©£¬ĪŽ³ōĪŽĪ¶”£ŌŚĖįŠŌĢõ¼žĻĀµāĖį¼ŲŹĒŅ»ÖÖ½ĻĒæµÄŃõ»Æ¼Į£¬ÓėĒāµāĖį”¢¶žŃõ»ÆĮņµČ»¹ŌŠŌĪļÖŹ×÷ÓĆ£¬±»»¹ŌĪŖµ„ÖŹµā£¬ŌŚ¼īŠŌ½éÖŹÖŠ£¬µāĖį¼ŲÄܱ»ĀČĘų”¢“ĪĀČĖįŃĪµČŃõ»ÆĪŖøßµāĖį¼Ų”£µāĖį¼ŲŌŚ³£ĪĀĻĀĪČ¶Ø£¬¼ÓČČÖĮ560 ”ęæŖŹ¼·Ö½ā”£¹¤ŅµÉś²śµāĖį¼ŲµÄĮ÷³ĢČēĻĀĶ¼ĖłŹ¾”£
²éæ““š°øŗĶ½āĪö>> æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2010-2011ѧğ¹ć¶«Ź”øßČżĮŁĆÅŅ»½Å×ŪŗĻ²āŹŌ£ØĄķ×Ū£©»Æѧ²æ·Ö ĢāŠĶ£ŗĢīæÕĢā KIO3ŌŚĖįŠŌĢõ¼žĻĀŹĒŅ»ÖÖ½ĻĒæµÄŃõ»Æ¼Į£¬ŌŚ¼īŠŌ½éÖŹÖŠÄܱ»Cl2”¢“ĪĀČĖįŃĪŃõ»ÆĪŖKIO4”£KIO3ŌŚ³£ĪĀĻĀĪČ¶Ø£¬¼ÓČČÖĮ560”ęæŖŹ¼·Ö½ā”£¹¤ŅµÉś²śKIO3µÄĮ÷³ĢČēĻĀ£ŗ
£Ø1£©Š“³ö·“Ó¦Ę÷ÖŠÉś³ÉKH£ØIO3£©2µÄ»Æѧ·½³ĢŹ½£ŗ 6I2+11KClO3+3H2O= ”£ µ±ÓŠ1£®2 molµē×Ó×ŖŅʵď±ŗņ£¬Éś³ÉKH£ØIO3£©2µÄĪļÖŹµÄĮæĪŖ ”£ £Ø2£©Éś²ś¹ż³ĢÖŠ£¬ŌŚ·“Ó¦Ę÷ÖŠ¼ÓČė·“Ó¦ĪļÖ®ŗ󣬻¹Šč¼ÓČėĻõĖįĖį»Æ²¢±£³ÖĪ¢·Š1Š”Ź±£¬¼ÓĻõĖįµÄÄæµÄŹĒ ”£Ī¢·Š1Š”Ź±µÄÄæµÄŹĒ ”£ £Ø3£©µ÷pH=10Ź±£¬Ėł¼ÓŹŌ¼ĮC×īŗĆŹĒ ”£ A£®NaOH B£®NH3”¤H2O C£®KOH D£®KCI £Ø4£©“ÓČÜŅŗBÖŠµĆµ½µāĖį¼Ų¹ĢĢ壬½ųŠŠµÄ²Ł×÷I°üĄØ ”£ A£®Õō·¢ÅØĖõ B£®ĄäČ“½į¾§ C£®Õō·¢½į¾§ D£®¹żĀĖĻ“µÓ
²éæ““š°øŗĶ½āĪö>> Ķ¬²½Į·Ļ°²į“š°ø °Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com°ęČØÉłĆ÷£ŗ±¾Õ¾ĖłÓŠĪÄÕĀ£¬Ķ¼Ę¬Ą“Ō“ÓŚĶųĀē£¬Öų×÷Čؼ°°ęČعéŌ×÷ÕßĖłÓŠ£¬×ŖŌŲĪŽŅāĒÖ·ø°ęČØ£¬ČēÓŠĒÖČØ£¬Ēė×÷ÕßĖŁĄ“ŗÆøęÖŖ£¬ĪŅĆĒ½«¾”æģ“¦Ąķ£¬ĮŖĻµqq£ŗ3310059649”£ ICP±ø°øŠņŗÅ: »¦ICP±ø07509807ŗÅ-10 ¶õ¹«Ķų°²±ø42018502000812ŗÅ |