
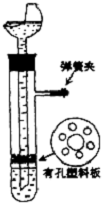
 用如图的装置制取氢气,在塑料隔板上放粗锌,漏斗和带支管的试管中装有稀硫酸,若打开弹簧夹,则硫酸由漏斗流下,试管中液面上升与锌粒接触,发生反应,产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止.需要时再打开弹簧夹,又可以使氢气发生.这是一种适用于室温下随制随停的气体发生装置.
用如图的装置制取氢气,在塑料隔板上放粗锌,漏斗和带支管的试管中装有稀硫酸,若打开弹簧夹,则硫酸由漏斗流下,试管中液面上升与锌粒接触,发生反应,产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止.需要时再打开弹簧夹,又可以使氢气发生.这是一种适用于室温下随制随停的气体发生装置.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:800mL烧杯、100mL量筒、短颈漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/L)、水.按图示装置进行实验,回答下列问题.(设合金样品完全反应,产生的气体体积不超过100mL)
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:800mL烧杯、100mL量筒、短颈漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/L)、水.按图示装置进行实验,回答下列问题.(设合金样品完全反应,产生的气体体积不超过100mL)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BaCl2溶液 |
| B、BaCl2溶液、稀盐酸 |
| C、BaCl2溶液、稀硝酸 |
| D、BaCl2溶液、稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com