
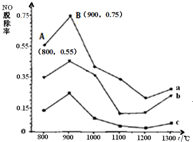
 一定条件下,尿素[CO(NH2)2]与NO反应生成N2和另外2种对环境无污染的氧化物.如图是CO(NH2)2与某种烟气中NO的物质的量之比分别为1:2、2:1、3:1时,NO脱除率随温度(t)变化的图象.下列说法错误的是( )
一定条件下,尿素[CO(NH2)2]与NO反应生成N2和另外2种对环境无污染的氧化物.如图是CO(NH2)2与某种烟气中NO的物质的量之比分别为1:2、2:1、3:1时,NO脱除率随温度(t)变化的图象.下列说法错误的是( )| A、尿素脱除NO的反应为:2CO(NH2)2+6NO═2CO2+4H2O+5N2 |
| B、图中a,对应CO(NH2)2与NO的物质的量之比为1:2 |
| C、在900℃左右,NO的脱除率最佳 |
| D、NO的起始浓度为6×10-4mg/m3,图中a从A点到B点经过0.8s,这段时间内NO的脱除平均速率为1.5×10-4mg/(m3?s) |
| 浓度变化量 |
| 时间 |
| 1.2×10-4mg/m3 |
| 0.8s |


科目:高中化学 来源: 题型:
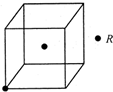 现有X、Y、Z、W、R五种元素,其中前四种为短周期主族元素.X原子的最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价的代数和为6;X、Z同主族,W与X、Y均不同周期,R2+的价电子排布式为3d5.
现有X、Y、Z、W、R五种元素,其中前四种为短周期主族元素.X原子的最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价的代数和为6;X、Z同主族,W与X、Y均不同周期,R2+的价电子排布式为3d5.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O和Na2O2的混合物共1mol,阴离子数目为NA |
| B、过量的Fe与Cl2反应生成0.1mol产物时失去的电子数为0.2NA |
| C、标准状况下,11.2 L CHCl3中含有C-Cl键的数目为1.5NA |
| D、一定条件下,2mol H2和0.5mol N2充分反应后可得到NH3分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性氢氧燃料电池的正极反应:H2-2e-+2OH-═2H2O | ||||
B、用电子式表示NaCl的形成过程: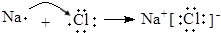 | ||||
| C、向含有Hg2+的废水中加入Na2S可除去Hg2+:Hg2++S2-═HgS↓ | ||||
D、汽车尾气系统的催化转化器可降低NO等的排放:2CO+2NO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量氯气通入溴化亚铁溶液中:2Cl2+2Fe2++2Br-═4Cl-+2Fe3++Br2 |
B、向苯酚溶液中滴加Na2CO3溶液: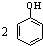 +CO32-→ +CO32-→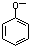 +CO2↑+H2O +CO2↑+H2O |
| C、足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- |
| D、用过量的冷氨水吸收SO2:SO2+2NH3?H2O═SO32-+2NH4++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
| B、在强酸溶液中:Na+、ClO-、Cl-、Ba2+ |
| C、在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、SCN- |
| D、由水电离的c(H+)=10-13mol?L-1的溶液中:Na+、Cl-、K+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
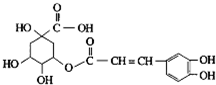 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )| A、绿原酸的分子式为C16H8O9 |
| B、1mol绿原酸最多与4mol NaOH反应 |
| C、1个绿原酸分子中含有4个手性碳原子 |
| D、绿原酸分子中有4种化学环境不同的氢原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、恒容密闭容器中进行反应:2A2(g)+B2(g)?2A2B(g);△H<0,达到化学平衡后,加热会使逆反应速率大于正反应速率 |
| B、在常温下,用惰性电极电解饱和Na2CO3溶液,Na2CO3溶液的浓度不变 |
| C、使用催化剂能够改变反应历程,增大反应物分子的接触面积,从而加快反应速率 |
| D、放热或熵增过程自发进行的可能性比吸热或熵减过程要大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质及其水解产物都具有两性 |
| B、淀粉和油脂都是可水解的高分子化合物 |
| C、鸡蛋清溶液中加入饱和Na2SO4溶液有沉淀生成是因为蛋白质变性 |
| D、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com