
(5分)在元素周期表中,元素的金属性和非金属性及其强弱比较与周期数(n)和主族数(A)有如下经验公式:K=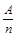 (K为A与n的比值)。请用编号回答下列问题:
(K为A与n的比值)。请用编号回答下列问题:
A.两性 B.金属 C.非金属 D.稀有气体
(1)当n一定时,K值越大,则元素的_____性越强
(2)当A一定时,K值越小,则元素的_____性越强
(3)当K=0,则该元素系_____元素,当K=l时(n≠1),则该元素系_____元素,当K<1时,该元素系____元素
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
A—F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示:
| 元素 | 结构或性质 |
| A | 原子最外层电子数是内层电子总数的1/5 |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
请回答下列问题:
(1)A在元素周期表中的位置是 ;A与E形成的化合物的电子式是 。
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是 。
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是 。
(4)F的盐酸盐水溶液呈酸性,原因是 (用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是 。
(5)A与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中A元素的含量。(装置中因空气质量引起的误差忽略不计)

①实验需要测定三个物理量:合金的质量m以及a和b。
a是 ;
b是 。
②合金中A元素的质量分数是 (用含m、a、b的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省孝感高级中学高二上学期期末考试化学试卷(带解析) 题型:单选题
下列说法正确的是
| A.在我们常用的元素周期表中,元素被划分为两类:金属元素和非金属元素 |
| B.在元素周期表中,每个纵列的价电子层的电子总数一定相等 |
| C.在元素周期表里,主族元素所在的族序数等于原子核外电子数 |
| D.在元素周期表中,s区,d区和ds区的元素都是金属元素 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市东城区高三上学期期末统一练习化学试卷(解析版) 题型:填空题
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等。
|
|
Q |
R |
|
|
T |
|
|
W |
(1)T的原子结构示意图是______。用化学方程式表示工业常用冶炼T单质的原理是______。
(2)与W同主族的某元素,其氢化物分子中含有18个电子,该分子中存在的共 价键的类型是______。
(3)元素的非金属性:Q______W(填“强于”或“弱于”),结合方程式简述其原因是______。
(4)甲是R的氧化物,通常状况下呈红棕色。现有一试管甲,欲使元素R全部转化为其最高价氧化物对应水化物,实验步骤:将盛有甲的试管倒扣在水槽中,______。
查看答案和解析>>
科目:高中化学 来源:2010-2011年江苏省高一下学期期末考试化学试卷 题型:填空题
工业上制取冰晶石(Na3AlF6)的化学方程式如下,
2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2↑+ 9H2O,根据题意完成下列填空:
(1)在上述反应的反应物和生成物中,属于非电解质的物质的电子式为 ,属于弱酸的电离方程式 。
(2)上述反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(3)上述反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。
(4)上述产物当中有一个物质比同族元素类似化合物的沸点高很多,写出这个物质的结构式_______,其沸点较高的原因是_______________;反应物中属于盐的物质中含有的化学键有________________。(填“离子键”或“共价键”或“金属键”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com