
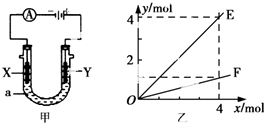
| A�� | ����װ�����ڵ�⾫��ͭ����XΪ��ͭ��YΪ��ͭ��������Һa����������ͭ���Ȼ�ͭ��Һ | |
| B�� | ��ͼ��װ���ö��Ե缫���AgN03��Һ����ͼ�Һ�����x��ʾ����缫�ĵ��ӵ����ʵ�������E�ɱ�ʾ��Ӧ������������ʵ�����F��ʾ���������������ʵ��� | |
| C�� | ��ͼ��װ���ö��Ե缫���һ��Ũ�ȵ�����ͭ��Һ��ͨ��һ��ʱ�����0.5mol��̼��ͭ�պûָ���ͨ��ǰ��Ũ�Ⱥ�pH�����������ת�Ƶĵ���Ϊ2.0 mol | |
| D�� | ��X��YΪ���缫��a��ҺΪ500 mL KCl��KNO3�Ļ��Һ������һ��ʱ����������õ���״����11.2 L���壬��ԭ���Һ��KCl�����ʵ���Ũ������Ϊ2.0 molL-1 |
���� A����⾫��ͭ����ͭ����������ͭ�������������ҺΪ����ͭ���ӵ���Һ��
B���������ĵ�ⷽ��ʽΪ��4AgNO3+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$O2��+4HNO3+4Ag�����ݷ���ʽ�жϣ�
C�����ݡ�����ʲô����ʲô���ķ���֪���������ͭ��Һʱ����������������ͭ������ԭ���غ�֪��0.5mol��̼��ͭ��ͭԪ�ص����ʵ�����0.5mol�������ϵĵ缫��ӦʽΪ��Cu2++2e-=Cu����ϵ����غ㣻
D�����500 mL KCl��KNO3�Ļ��Һ�������������ӷŵ�����������2Cl--2e-=Cl2���������������ӷŵ������������������õ���״����11.2 L��0.5mol���壬����ԭ���غ���㣮
��� �⣺A����⾫��ͭ����ͭ����������ͭ����������YΪ��ͭ��XΪ��ͭ��������Һa����������ͭ���Ȼ�ͭ��Һ����A��ȷ��
B���������ĵ�ⷽ��ʽΪ��4AgNO3+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$O2��+4HNO3+4Ag�����ݷ���ʽ֪����ת��4mol����ʱ����1mol������4mol���ᣬ��ͼ���Ǻϣ���B��ȷ��
C�����ݡ�����ʲô����ʲô���ķ���֪���������ͭ��Һʱ����������������ͭ������ԭ���غ�֪��0.5mol��̼��ͭ��ͭԪ�ص����ʵ�����0.5mol�������ϵĵ缫��ӦʽΪ��Cu2++2e-=Cu����������0.5molͭ��Ҫת�Ƶ��ӵ����ʵ�����1mol����C����
D�����500 mL KCl��KNO3�Ļ��Һ�������������ӷŵ�����������2Cl--2e-=Cl2���������������ӷŵ������������������õ���״����11.2 L��0.5mol���壬���������ӵ����ʵ�����1mol���Ȼ��ص����ʵ�����1mol������KCl��Ũ����$\frac{1mol}{0.5L}$=2mol/L����D��ȷ��
��ѡC��
���� ���⿼���˵��ԭ����Ӧ�ã���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͼ���������ע����յ��������������Ϸ����ķ�Ӧ�Լ������غ��ڼ����е�Ӧ�ã�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | �Լ� | ���������� |
| A | AgNO3��Һ | �μӰ�ˮ�����������������μӰ�ˮ�������ܽ� |
| B | ���� | �μ�NaOH��Һ���������壻�����μӣ�������ɫ���� |
| C | CuSO4��Һ | �ӹ���NaOH��Һ��������ɫ�������ټ���ȩ�����ȣ�������ɫ���� |
| D | ��ˮ | �μ�NaOH��Һ����Һ��ɫ��ȥ���ټ�HCl����Һ��ɫ�ָ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
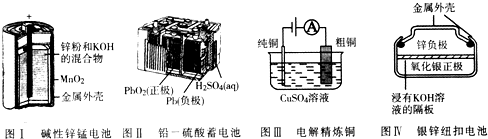
| A�� | ͼI��ʾ����У�п���缫��ӦΪZn-2e-�TZn2+ | |
| B�� | ͼ����ʾ��طŵ�����У�ÿת��1mo1���ӣ�����1mol PbSO4 | |
| C�� | ͼIII��ʾװ�ù��������У��������Һ��Cu2+Ũ��ʼ�ղ��� | |
| D�� | ͼ����ʾ����У�Ag2O�ڵ�ع��������б�����ΪAg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ������Һ�У�Na+��MnO4-��NO3-��Br- | |
| B�� | 0.1 mol•L-1CaCl2��Һ�У�Mg2+��NH4+��CO32-��SO42- | |
| C�� | Kw/c��OH-��=10-12 mol•L-1����Һ��Na+��K+��SiO32-��Cl- | |
| D�� | ˮ���������c��H+��=10-12 mol•L-1����Һ�У�K+��Fe2+��NO3-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
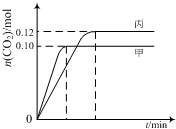 һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��2NO��g��+2CO��g��?N2��g��+2CO2��g��
һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��2NO��g��+2CO��g��?N2��g��+2CO2��g��| ���� | �¶�/�� | ��ʼ���ʵ���/mol | |
| NO ��g�� | CO ��g�� | ||
| �� | T1 | 0.20 | 0.20 |
| �� | T1 | 0.30 | 0.30 |
| �� | T2 | 0.20 | 0.20 |
| A�� | �÷�Ӧ������ӦΪ���ȷ�Ӧ | |
| B�� | �ﵽƽ��ʱ������CO2����������ȼ��е�С | |
| C�� | T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2����Ӧ�ﵽ��ƽ��ǰv��������v���棩 | |
| D�� | T2��ʱ������ʼʱ����г���0.06mol N2��0.12 mol CO2�����ƽ��ʱN2��ת���ʴ���40% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ķǽ����Ա�̼ǿ | |
| B�� | SO2��������ͨ��NaHCO3��Һ������ʯ��ˮ������ʯ��ˮ����� | |
| C�� | SO2��CO2����ֱ�ͨ��ˮ�������ͣ��ⶨ����Һ��pH��ǰ��С�ں��� | |
| D�� | �����²ⶨ��Ϊ0.1mol/L��NaHSO3��NaHCO3��Һ��pH��ǰ��С�ں��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | ���������� | ���� |
| A | ����ˮ�м��������������ú�ˮ��Ϊ��ɫ | ����Br2�����˼ӳɷ�Ӧ |
| B | ��ij��ɫ��Һ�еμ������ữ��BaCl2��Һ��������ɫ���� | ԭ��Һ��һ������SO42- |
| C | ��25mL��ˮ�ͷ�ˮ�зֱ����5��FeCl3������Һ��ǰ��Ϊ��ɫ������Ϊ���ɫ | �¶����ߣ�Fe3+��ˮ��̶����� |
| D | ��1mL KSCN��Һ��1mL ͬŨ��FeCl3��Һ��ֻ�ϣ��ټ�������KSCN��Һ����Һ��ɫ���� | ֤����Һ�д���ƽ�⣺Fe3++3SCN?Fe��SCN��3 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
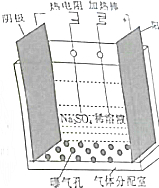 ����������ʵ���ҳ��õ��Լ�����ҽ�ơ����¼���ҵ����;Ҳ�dz��㷺���ش��������⣺
����������ʵ���ҳ��õ��Լ�����ҽ�ơ����¼���ҵ����;Ҳ�dz��㷺���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�ϵ�һ���ʼ컯ѧ���������棩 ���ͣ�ѡ����
ij����A��һ�������¼��ȷֽ⣬����ȫ�����塣A�ķֽⷴӦΪ��2A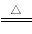 B+2C+2D���ֲ�÷ֽ�����Ļ��������ܶ���������d������A����Է�����Ϊ
B+2C+2D���ֲ�÷ֽ�����Ļ��������ܶ���������d������A����Է�����Ϊ
A��2d B��2.5 C��5d D��0.8d
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com