
【题目】氧化钡广泛用于玻璃、陶瓷工业,是制取过氧化钡和钡盐的原料。一种利用钡泥[含BaCO3、BaSO3、Ba(FeO2)2等]制取氧化钡的绿色工艺流程如下:
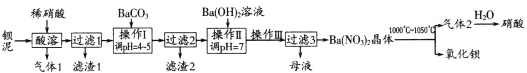
回答下列问题:
(1)酸溶时,Ba(FeO2)2与稀硝酸反应的化学方程式为_____________________。
(2)产生滤渣1的反应离子方程式是____________________________________________。
(3)操作Ⅰ调pH=4~5的目的是_________________________________________________。
(4)过滤3所得母液应返回______________工序循环使用。
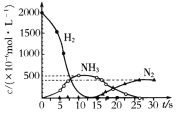
(5)Ba(NO3)2可用于汽车尾气中还原性气体的催化转化。科技工作者用H2模拟尾气中的还原性气体,研究Ba(NO3)2的催化还原过程。该过程分两步进行,如图表示该过程相关物质浓度随时间的变化关系。第二步反应消耗的NH3与NO3-的物质的量之比是_________。
(6)“气体2”为混合气体。标准状况下a L“气体2”溶于水得到bL溶液,则所得溶液的物质的量浓度为_________________
【答案】Ba(FeO2)2+8HNO3= Ba(NO3)2+2Fe(NO3)3+4H2O 3BaSO3+2H++2NO3-= 3BaSO4+2NO↑+H2O 将Fe3+转化成Fe(OH)3沉底而除去 操作Ⅱ 5:3 ![]()
【解析】
钡泥加入稀硝酸时,碳酸钡生成硝酸钡和二氧化碳和水,亚硫酸钡生成硫酸钡、NO和水,Ba(FeO2)2生成硝酸钡、硝酸铁和水,则气体1 为二氧化碳,滤渣1为硫酸钡;加入碳酸钡调节pH,可使铁离子生成氢氧化铁沉淀,则滤渣2为氢氧化铁;加入氢氧化钡中和溶液中过量的硝酸,生成硝酸钡溶液,则母液为硝酸钡;加热硝酸钡晶体可生成氧化钡、二氧化氮和氧气。
(1)酸溶时,硝酸可使FeO2-生成铁离子和水,反应的方程式为Ba(FeO2)2+8HNO3= Ba(NO3)2+2Fe(NO3)3+4H2O;
(2)硝酸具有强氧化性,能够使亚硫酸钡变为硫酸钡,同时生成NO气体,离子方程式为3BaSO3+2H++2NO3-= 3BaSO4+2NO↑+H2O;
(3)操作Ⅰ调pH=4~5,中和过量的硝酸,使溶液中的铁离子生成氢氧化铁沉淀;
(4) 过滤3所得母液为饱和的硝酸钡溶液,可加入到操作II中,继续使用,提高硝酸钡的产率;
(5)根据图像可知,第二步反应为NH3与NO3-反应生成氮气,发生反应的方程式为5NH3+3NO3-+3H+=4N2+9H2O,则消耗的NH3与NO3-的物质的量之比为5:3;
(6)硝酸钡受热分解生成氧化钡、二氧化氮和氧气,方程式为2Ba(NO3)2![]() 2BaO+4NO2↑+O2↑,标准状况下a L此混合气体溶于水可生成硝酸,其中
2BaO+4NO2↑+O2↑,标准状况下a L此混合气体溶于水可生成硝酸,其中![]() 为NO2,则生成硝酸的物质的量为
为NO2,则生成硝酸的物质的量为![]() mol,c=
mol,c=![]() mol/L。
mol/L。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】物质A、B、C、D、E、F、G、H、I、J、K存在下图转化关系,其中气体D、E为单质,试回答:
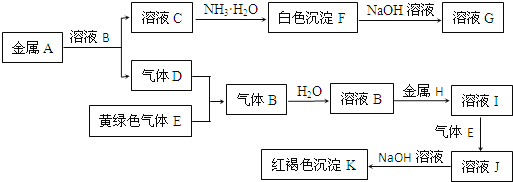
(1)写出下列物质的化学式:
A是_______________,D是___________,K是_______________。
(2)写出反应“C→F”的离子方程式:_______________________。
(3)写出反应“F→G”的化学方程式:_______________。
(4)在溶液I中滴入NaOH溶液,可观察到的现象是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 若单位时间内生成xmolNO的同时消耗xmolNH3,则反应达到平衡状态
B. 化学反应速率关系是:2v正(NH3)=3v正(H2O)
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 达到化学平衡时,4v正(O2)=5v逆(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二硫代磷酸锌( ![]() )是一种表面活性剂,能够提高橡胶的抓着力、耐磨性。请回答下列问题:
)是一种表面活性剂,能够提高橡胶的抓着力、耐磨性。请回答下列问题:
(1)二硫代磷酸锌结构中,P的杂化方式为__________________,C1、P、S的第一电离能由大到小的顺序为_____________________。
(2)Zn2+的价层电子排布式为________________,锌能够跟强碱溶液反应生成[Zn(OH)4]2-,不考虑空间构型,[Zn(OH)4]2-的结构可用示意图表示为__________________。
(3)硫元素能形成多种含氧酸,两分子硫酸脱去一分子水生成焦硫酸(H2S2O7),则1mol焦硫酸中含有硫氧键的数目为____________;用价层电子互斥理论判断并解释SO32-与SO42-键角的相对大小。
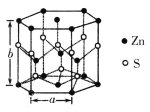
(4)纤锌矿的六方晶体结构如图所示,该晶胞的化学式为___________,其晶胞参数分别为a pm和b pm,则该晶体的密度为____________________g·cm-3(用含a、b、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
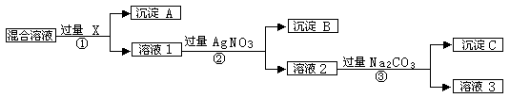
请回答下列问题:
⑴写出实验流程中下列物质的化学式: 试剂X : ,沉淀A:
⑵上述实验流程中加入过量的Na2CO3的目的是 。
⑶按此实验方案得到的溶液3中肯定含有 (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的 ,之后若要获得固体NaNO3需进行的实验操作是 (填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,综合利用CO2对构建低碳社会有重要意义。
(1)已知: H2(g)+ ![]() O2(g) =H2O(g) ΔH=-241.8kJ·mol-1 CO2(g) = CO(g)+
O2(g) =H2O(g) ΔH=-241.8kJ·mol-1 CO2(g) = CO(g)+ ![]() O2(g) ΔH=+283.0kJ·mol-1 则反应:CO2(g)+H2O(g) =CO(g)+H2(g)+O2(g) ΔH=________。
O2(g) ΔH=+283.0kJ·mol-1 则反应:CO2(g)+H2O(g) =CO(g)+H2(g)+O2(g) ΔH=________。
(2)工业生产中可利用H2还原CO2制备清洁能源甲醇:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH<0
CH3OH(g)+H2O(g) ΔH<0
①保持温度、体积一定,能说明上述反应达到平衡状态的是_________。
A.容器内压强不变 B.3v正 (CH3OH)= v正 (H2)
C.容器内气体的密度不变 D.CO2与H2O的物质的量之比保持不变
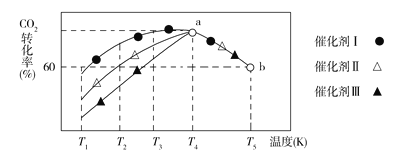
②将一定量的CO2和H2充入到某恒容密闭容器中,测得在不同催化剂作用下,相同时间内CO2的转化率随温度的变化如图所示,催化效果最好的是催化剂________(填“Ⅰ”“Ⅱ”或“Ⅲ”),该反应在a点达到平衡状态,a点的转化率比b点的高,其原因是________。
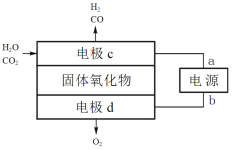
(3)固体氧化物电解池(SOEC)可用于高温电解CO2/H2O,既可高效制备合成气(CO和H2),又可实现CO2的减排,其工作原理如图。
①电源正极为________(填“a”或“b”),电极c上发生的电极反应式为________、_____。
②阴阳两极生成的气体的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某化学反应的平衡常数表达式为K=[c(CO2)·c(H2)] /[c(CO)·c(H2O)],在不同的温度下该反应的平衡常数值分别为:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述错误的是
A. 该反应的化学方程式是:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B. 上述反应的正反应是放热反应
C. 如果在1L的密闭容器中加入CO2和H2各1mol,再把温度升高到830℃,此时测得CO2为0.4 mol时,该反应达到平衡状态
D. 若平衡浓度关系符合c(CO2)/3c(CO)=c(H2O)/5c(H2),可判断此时温度是1000℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com