
(14分)由软锰矿(主要成分为MnO2)制备KMnO4的实验流程可表示如下:
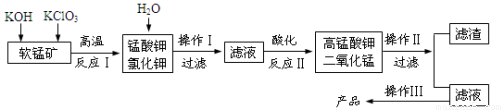
(1)反应Ⅰ发生反应的化学方程式是 ;
反应Ⅱ发生反应的离子方程式是 ;
(2)操作Ⅲ的实验步骤为 、 ;可循环利用的物质的化学式为 ;
(3)计算用2.5kg含MnO280%的软锰矿制备,理论上可得KMnO4为 :
(4)取制得的产品6.5g,配成250mL溶液;准确称取纯Na2C2O41.34g配成适量溶液。用上述KMnO4溶液滴定Na2C2O4溶液,恰好反应(氧化产物为CO2,还原产物为Mn2+)时,消耗KMnO4溶液的体积为25.00mL。该KMnO4的纯度为 %(保留小树点后一位)。
(1)3MnO2+KClO3+6KOH
 3K2MnO4+KCl+3H2O. (2分)
3K2MnO4+KCl+3H2O. (2分)
3MnO42-+4H+=MnO2↓+2MnO4-+2H2O (2分)
(2)浓缩(2分) 结晶(2分) MnO2 (2分)
(3)2.4kg (2分)
(4)97.2% (2分)
【解析】
试题分析:(1)根据题给流程知,KOH、KClO3、MnO2共熔制得K2MnO4、KCl,由原子守恒可知,还会生成H2O,反应方程式为:3MnO2+KClO3+6KOH 3K2MnO4+KCl+3H2O;由流程图可知,操作Ⅰ的滤液酸化生成高锰酸钾与二氧化锰,应是锰酸根与氢离子反应生成二氧化锰与高锰酸根离子,同时生成水,反应方程式为:3MnO42-+4H+=MnO2↓+2MnO4-+2H2O;(2)操作Ⅲ是从溶液中获得高锰酸钾晶体,应采取加热蒸发、冷却结晶等操作;操作Ⅱ的滤渣中含有二氧化锰,可以在反应Ⅰ中循环利用;(3)根据反应Ⅰ、Ⅱ,可以得出关系式3MnO2——2KMnO4,令理论上可得KMnO4为x kg,则87×3:2×158=2.5kg×80%:xkg,解得:x=2.4;(4)发生反应2KMnO4+5Na2C2O4+8H2SO4
3K2MnO4+KCl+3H2O;由流程图可知,操作Ⅰ的滤液酸化生成高锰酸钾与二氧化锰,应是锰酸根与氢离子反应生成二氧化锰与高锰酸根离子,同时生成水,反应方程式为:3MnO42-+4H+=MnO2↓+2MnO4-+2H2O;(2)操作Ⅲ是从溶液中获得高锰酸钾晶体,应采取加热蒸发、冷却结晶等操作;操作Ⅱ的滤渣中含有二氧化锰,可以在反应Ⅰ中循环利用;(3)根据反应Ⅰ、Ⅱ,可以得出关系式3MnO2——2KMnO4,令理论上可得KMnO4为x kg,则87×3:2×158=2.5kg×80%:xkg,解得:x=2.4;(4)发生反应2KMnO4+5Na2C2O4+8H2SO4 K2SO4+2MnSO4+5Na2SO4+10CO2↑+8H2O,令KMnO4的纯度为y,根据2KMnO4——5Na2C2O4代入题给数据计算 2×158:5×134=6.5g×y×0.1:1.34g解得y=97.2%。
K2SO4+2MnSO4+5Na2SO4+10CO2↑+8H2O,令KMnO4的纯度为y,根据2KMnO4——5Na2C2O4代入题给数据计算 2×158:5×134=6.5g×y×0.1:1.34g解得y=97.2%。
考点:以化学工艺流程为载体考查化学方程式、离子方程式的书写,化学实验基本操作,化学计算。


科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:选择题
下列有关物质性质、结构的表述均正确,且存在因果关系的是
表述Ⅰ | 表述Ⅱ | |
A | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
B | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1—与Na+间的作用力大于碘晶体中分子间的作用力 |
C | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
D | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
某温度下,可逆反应mA(g)+nB(g) pC(g)的平衡常数为K,下列对K的说法正确的是
pC(g)的平衡常数为K,下列对K的说法正确的是
A.K值越大,表明该反应越有利于C的生成,反应物的转化率越大
B.若缩小反应器的容积,能使平衡正向移动,则K增大
C.温度越高,K一定越大
D.如果m+n=p,则K=1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
如下图所示,△H1=-393.5 kJ?mol-1,△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是

A.C(s,石墨)== C(s,金刚石) △H= +1.9 kJ?mol-1
B.石墨和金刚石的转化是物理变化
C.金刚石的稳定性强于石墨
D.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧
C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期中考试化学试卷(解析版) 题型:选择题
①①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O,
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O,
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4。
下列结论正确的是
A.①②③均是氧化还原反应
B.氧化性强弱顺序是
C.反应②中氧化剂与还原剂的物质的量之比为6:1
D.反应③中0.1mol还原剂共失去电子数为
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期中考试化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化
B.铅蓄电池放电时铅电极发生氧化反应
C.胶体与溶液的分离可用渗析的方法
D.生铁浸泡在食盐水中发生析氢腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.常温条件下,11.2L甲烷气体含甲烷分子数为0.5NA
B.标准状况下,22.4L Cl2通入水中,反应过程中转移电子数为NA
C.常温条件下,0.1mol·L-1的氢氧化钠溶液中含钠离子数为0.1NA
D.标准状况下,16g O2和O3的混合气体中含氧原子数为NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期中化学试卷(解析版) 题型:选择题
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是
A.原子半径的大小顺序:rY> rX >rQ>rW
B.X、Y的最高价氧化物的水化物之间不能发生反应
C.Z元素的氢化物稳定性大于W元素的氢化物稳定性
D.元素Q和Z能形成QZ2型的共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com