
| A. | NH4Fe(SO4)2的溶液中:H+、Mg2+、Br-、NO3- | |
| B. | 含有大量HCO3-的溶液:NH4+、Ca2+、AlO2-、I- | |
| C. | 浓度为3%的H2O2溶液:H+、Fe2+、C1-、SO42- | |
| D. | c(S2-)=0.1mo1.L-1的溶液中:Na+、NH4+、ClO-、SO42- |
科目:高中化学 来源: 题型:选择题
| A. | 体积减半,则N2O4的浓度为原来的两倍 | |
| B. | 平衡向右移动,混合气体的颜色一定会变浅 | |
| C. | 体积减半,压强增大,但小于原来的2倍 | |
| D. | 平衡向右移动,但混合气体密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol丙烯酸中含有双键的数目为0.2NA | |
| B. | 丙烯和1-丁烯组成的21g混合气体中氢原子的个数为3NA | |
| C. | 标准状况下,11.2L苯中含有分子的数目为0.5NA | |
| D. | 1mol羟基与1mol氢氧根离子所含电子数均为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
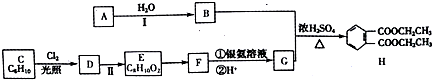
 等.
等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
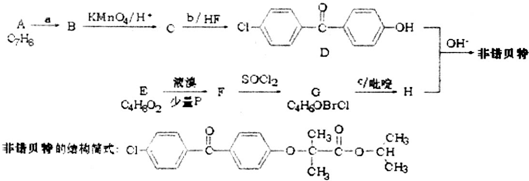
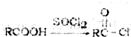
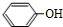 ,F
,F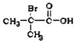 .
.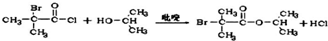 .
.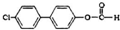 .
.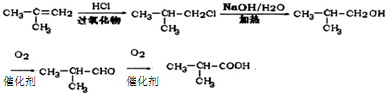 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
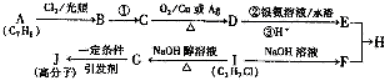
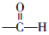 ,发生反应①的条件是氢氧化钠水溶液、加热.
,发生反应①的条件是氢氧化钠水溶液、加热. .
.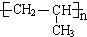 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
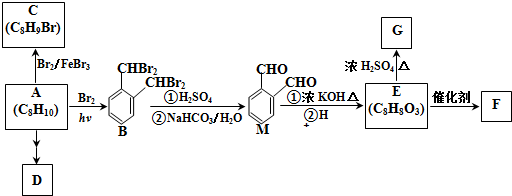

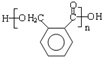 .由A生成B的反应过程中,会同时生成多种副产物,其中一种与B互为同分异构体,它的核磁共振氢谱有5个吸收峰.
.由A生成B的反应过程中,会同时生成多种副产物,其中一种与B互为同分异构体,它的核磁共振氢谱有5个吸收峰. .
.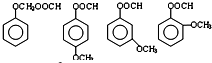 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
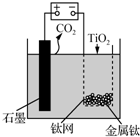 用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )
用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛.下列说法正确的是( )| A. | 电解过程中,Ca2+向阳极移动 | |
| B. | 阳极的电极反应式为:C+2O2--4e-═CO2↑ | |
| C. | 在制备金属钛前后,整套装置中CaO的总量减少 | |
| D. | 若用铅蓄电池作该装置的供电电源,“+”接线柱是Pb电极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com