

 试回答下列问题
试回答下列问题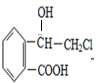 ,A发生消去反应生成B为
,A发生消去反应生成B为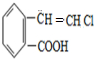 ,B再与氢气加成得C,C在碱性条件下水解得D为
,B再与氢气加成得C,C在碱性条件下水解得D为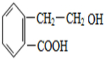 ,D发生分子内酯化得戊.
,D发生分子内酯化得戊. ,A发生消去反应生成B为
,A发生消去反应生成B为 ,B再与氢气加成得C,C在碱性条件下水解得D为
,B再与氢气加成得C,C在碱性条件下水解得D为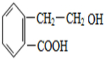 ,D发生分子内酯化得戊;
,D发生分子内酯化得戊;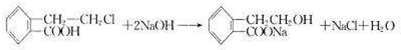 ,
, ;
;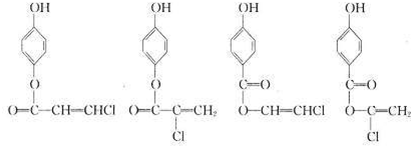 ,
,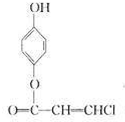 或
或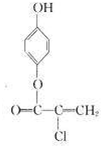 或
或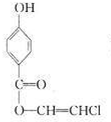 或
或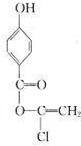 ;
;


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 ”表示硝基、用“…”表示氢键,画出C2分子的结构
”表示硝基、用“…”表示氢键,画出C2分子的结构 和
和  ,写出另3种同分异构体的结构简式
,写出另3种同分异构体的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
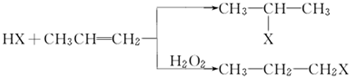
 的物质,该物质是一种香料.
的物质,该物质是一种香料.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | HX | HY | HZ | ||
| 浓度(mol/L) | 0.12 | 0.2 | 0.9 | 1 | 1 |
| 电离度 | 0.25 | 0.2 | 0.1 | 0.3 | 0.5 |
| 电离常数 | K1 | K2 | K3 | K4 | K5 |
| A、在相同温度,从HX的数据可以说明:弱电解质溶液,浓度越低,电离度越大,且K1>K2>K3=0.01 |
| B、室温时,若在NaZ溶液中加水,则c(Z-)/[c(HZ)?c(OH-)]的比值变小,若加少量盐酸,则比值变大 |
| C、等物质的量的NaX、NaY和NaZ的混合,c(X-)+c(Y-)-2c(Z-)=2c(HZ)-c(HX)-c(HY),且c(Z-)<c(Y-)<c(X-) |
| D、在相同温度下,K5>K4>K3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com