
 һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬������ӦFe��s��+CO2��g��?FeO��s��+CO��g����H��0��CO2��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
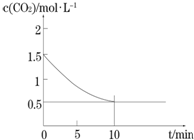
һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬������ӦFe��s��+CO2��g��?FeO��s��+CO��g����H��0��CO2��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ������ ���ȼ����ƽ�ⳣ��������̼��CO��Ũ�ȣ���������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ�ȵ��ݴη��˻��õ�ƽ�ⳣ������ʽ������ͼ�����ݼ�����K�����ݼ������ƽ�ⳣ��K��ʽ���������̼��ƽ��Ũ�ȣ�
��$\frac{c��CO��}{c��C{O}_{2}��}$�Ǹ÷�Ӧ��ƽ�ⳣ������ʽ��ƽ�ⳣ�����¶ȱ仯�����ƽ���ƶ�ԭ�������жϣ�
��� �⣺�پ�ͼ����ƽ��ʱ������̼��Ũ�ȷֱ�Ϊ0.5mol/L��������̼��Ũ�ȱ仯Ϊ��1.5mol/L-0.5mol/L=1mol/L�����ݷ�Ӧ����ʽ��֪��Ӧ����CO��Ũ��Ϊ1mol/L��
��÷�Ӧ��ƽ�ⳣ��K=$\frac{c��CO��}{c��C{O}_{2}��}$=$\frac{1.0mol/L}{0.5mol/L}$=2.0��
��CO2����ʼŨ��Ϊ2.0mol•L-1���ݷ���ʽ��֪����Ӧ�Ķ�����̼��Ũ��������COŨ����ȣ�����ߵ�Ũ��Ϊxmol/L��
��ƽ��ʱ������̼Ũ��Ϊ��2.0-x��mol/L��K=$\frac{c��CO��}{c��C{O}_{2}��}$=$\frac{x}{2.0-x}$=2.0��
��ã�x=$\frac{4}{3}$��
����ƽ��ʱ������̼Ũ��Ϊ����2.0-$\frac{4}{3}$��mol/L=$\frac{2}{3}$mol/L��
�ʴ�Ϊ��2.0��$\frac{2}{3}$��
��$\frac{c��CO��}{{c��C{O_2}��}}$Ϊ�÷�Ӧ��ƽ�ⳣ����ƽ�ⳣ�����¶ȱ仯������Ũ��ѹǿ�����ر仯����Ӧ�����ȷ�Ӧ������ƽ��ʱK����
A�������¶ȣ�ƽ��������У�ƽ�ⳣ������A��ȷ��
B������ѹǿ��ƽ�ⲻ����ƽ�ⳣ�����䣬��B����
C������һ����������̼��ƽ�����������ƶ��������¶Ȳ��䣬��ƽ�ⳣ�����䣬��C����
D������Ϊ���壬�ټ������ۺ�ƽ�ⲻ�����ƶ�����÷�Ӧ��ƽ�ⳣ�����䣬��D����
�ʴ�Ϊ��A��
���� ���⿼�������ʵ���Ũ����ʱ��仯�����ߣ���Ŀ�Ѷ��еȣ���ȷ��ѧƽ�⼰��Ӱ������Ϊ���ؼ�������������ѧ���ķ������������������Ӧ��������


 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ3NO2��g��+H2O��l��=2HNO3��aq��+NO��g���������¿��Է����У���÷�Ӧ�ġ�H��0 | |
| B�� | ��ͭ�ĵ�⾫�������У���ת��1mol���ӣ��������ܽ�32gCu | |
| C�� | ��������CuS������Һ�м��뱥��MnSO4��Һ������MnS��������Ksp��MnS������Ksp��CuS�� | |
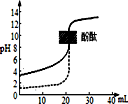
| D�� | ��������0.1mol/LNaOH��Һ�ֱ�ζ���ͬ���ʵ���Ũ�Ⱥ���ͬ���������ʹ��ᣬ����ʵ�ߣ���ͼ����ʾ���ǵζ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢ� | B�� | �ۢ� | C�� | �ۢܢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
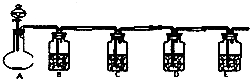 ���һʵ�齫ֻ����Na2SO4��Na2SO3��Na2CO3�İ�ɫ�����е����ֳɷּ��������ȡһ�����İ�ɫ��������ƿA�У�ͨ����Һ©������Һ��a����ͼ��ʾ��
���һʵ�齫ֻ����Na2SO4��Na2SO3��Na2CO3�İ�ɫ�����е����ֳɷּ��������ȡһ�����İ�ɫ��������ƿA�У�ͨ����Һ©������Һ��a����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
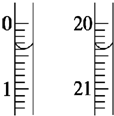 Ϊ�ⶨNa2S2O3•5H2O��Ʒ���ȣ�ȷ��ȡWg��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ������0.1000mol•L?1��ı���Һ�ζ��� ��Ӧԭ��Ϊ��2S2O32?+I2=S4O62-+2I?
Ϊ�ⶨNa2S2O3•5H2O��Ʒ���ȣ�ȷ��ȡWg��Ʒ������������ˮ�ܽ⣬�Ե�����ָʾ������0.1000mol•L?1��ı���Һ�ζ��� ��Ӧԭ��Ϊ��2S2O32?+I2=S4O62-+2I?�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 25��ʱ��pH=7��NH4Cl��NH3•H2O�����Һ�У�c��H+��=c��OH-����c��NH4+��=c��Cl-�� | |
| B�� | ��pH=3�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ����� | |
| C�� | ��Na2CO3��Һ����εμ�ϡ����ʱ����Һ��c��HCO3-���ı仯������ȱ�С���� | |
| D�� | 0.01 mol•L-1Na2CO3��Һ��0.01 mol•L-1 NaHCO3��Һ�������ϣ�3c��CO32-��+3c��HCO3-��+3c��H2CO3��=2c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
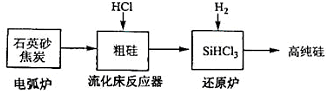
| ��������Ҫ��Ӧ | |
| �绡¯ | SiO2+2C$\stackrel{1600-1800��}{?}$Si+2CO�� |
| ���������� | Si+3HCl$\stackrel{250-300��}{?}$SiHCl3+H2 |
| ��ԭ¯ | SiHCl3+H2$\stackrel{1100-1200��}{?}$Si+3HCl |
| ���� | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| �е�/�� | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
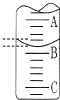 ij��ѧʵ��С����Ҫ�˽��г�����ʳ�ð״ף���Ҫ�Ǵ����ˮ��Һ����ȷŨ�ȣ��ִ��г�������һƿijƷ��ʳ�ð״ף���ʵ���ұ�NaOH��Һ������еζ���
ij��ѧʵ��С����Ҫ�˽��г�����ʳ�ð״ף���Ҫ�Ǵ����ˮ��Һ����ȷŨ�ȣ��ִ��г�������һƿijƷ��ʳ�ð״ף���ʵ���ұ�NaOH��Һ������еζ���| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ����NaOH��Һ���/mL | 26.02 | 25.35 | 25.30 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com