
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在a g HmX中所含质子的物质的量是 ( )
A.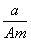 (A-N+m)mol B.
(A-N+m)mol B.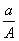 (A-N)mol
(A-N)mol
C.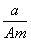 (A-N)mol D.
(A-N)mol D.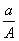 (A-N+m)mol
(A-N+m)mol
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.化学键的极性越大,键就越强
B.凡能形成氢键的物质,其熔、沸点比同类物质的熔、沸点高
C.CFH3分子中,既有H原子,又有电负性大、半径小的F原子,因此,CFH3分子间可以形成氢键
D.稀有气体能在温度充分降低时液化,而且随相对分子质量的增大熔点升高
查看答案和解析>>
科目:高中化学 来源: 题型:
用下面的方案进行某些离子的检验,其中方案设计最严密的是( )
A.检验试液中的SO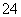 :试液
:试液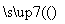 无沉淀
无沉淀 白色沉淀
白色沉淀
B.检验试液中的SO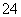 :试液
:试液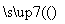 无沉淀
无沉淀 白色沉淀
白色沉淀
C.检验试液中的I-:试液 深黄色溶液
深黄色溶液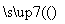 深黄色溶液
深黄色溶液
D.检验试液中的CO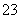 :试液
:试液 白色沉淀
白色沉淀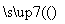 沉淀溶解
沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关硫元素及其化合物的说法或描述正确的是( )
A.硫黄矿制备硫酸经历两步:S SO3
SO3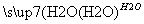 H2SO4
H2SO4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O2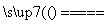 2CO2+2CaSO4
2CO2+2CaSO4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是________(填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是__________(填化学式),反应的化学方程式为________________________________________________________________________。
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有____(填字母)。
A.酸性 B.吸水性
C.脱水性 D.强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液____________,说明这种气体具有__________性;将(2)中产生的有刺激性气味的气体通入水中可生成一种不稳定、易分解的酸,请写出该反应的化学方程式:_________________________。
(5)能否用澄清石灰水鉴别这两种气体?________(填“能”或“不能”),若不能,请填写两种能鉴别的试剂____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求填空(均为短周期元素)
(1)最外层电子数为1的元素有______(填元素符号,下同)。
(2)最外层电子数为2的元素有______。
(3)最外层电子数与次外层电子数相等的元素有______。
(4)最外层电子数是次外层电子数2倍的元素是______。
(5)最外层电子数是次外层电子数3倍的元素是______。
(6)次外层电子数是最外层电子数2倍的元素有______。
(7)内层电子总数是最外层电子数2倍的元素有______。
(8)电子层数与最外层电子数相等的元素有______。
(9)最外层电子数是电子层数2倍的元素有______。
(10)最外层电子数是电子层数3倍的元素有______。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):

(1)如果A、B、C、D均是10电子的粒子,请写出A、D的电子式:A____________;D____________。
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式为__________________________________________。
②根据上述离子方程式,可以判断C与B结合质子的能力大小是________________________________________________________________________
________________________________________________________________________
(用化学式或离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的  ,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。
,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。
请回答下列问题:
(1)B单质的电子式是________。
(2)A、B、C、E可形成两种酸式盐(均由四种元素组成),两种酸式盐相互反应的离子方程式为____________________________。
(3)A、C、E间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定质量的铁和足量的稀硝酸或浓硝酸完全反应,在相同条件下,用排水集气法收集产生的气体。下列叙述一定正确的是( )
①硝酸浓度越大,消耗的硝酸越少
②硝酸浓度不同,生成的Fe(NO3)3的物质的量相同
③硝酸浓度越大,产生的气体越少
④用排水集气法收集到的气体在相同状况下体积相同
A.只有② B.②④
C.③④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com