
 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
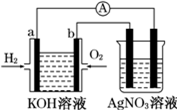
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.分析 (1)氢氧燃料电池工作时,通入氢气的电极为负极,发生氧化反应,在碱性溶液中,电极方程式为H2-2e-+2OH-=2H2O,通入氧气的电极为正极,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,总反应式为2H2+O2=2H2O,电解硝酸银溶液,pH减小;
(2)电解硝酸银溶液,阴极发生4Ag++4e-=4Ag,阳极发生4OH--4e-=2H2O+O2↑,总反应式为4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4HNO3+O2↑+4Ag,根据方程式判断.
解答 解:(1)A、a电极通入氢气,发生氧化反应,应是负极,原电池工作时OH-移向负极,故A正确;
B、通入氧气的b电极为正极,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,故B正确;
C、电极总反应式为2H2+O2=2H2O,不是在点燃的条件下反应,故C错误;
D、电解硝酸银溶液总反应式为4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4HNO3+O2↑+4Ag,电池中电解质溶液的pH减小,故D错误;
E、氢氧燃料电池可分别在两级上通入氢气和氧气,是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置,故E正确.
故答案为:CD;
(2)电解硝酸银溶液,阴极发生4Ag++4e-=4Ag,阳极发生4OH--4e-=2H2O+O2↑,总反应式为4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4HNO3+O2↑+4Ag,所以电解一段时间后溶液pH减小,故答案为:减小.
点评 本题考查电化学知识,为高考常见题型,侧重于考查学生综合运用化学知识的能力和分析问题的能力,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 2H2O(g)=2H2(g)+O2(g)△H=+483.6KJ/mol | |
| B. | H2的燃烧热为241.8 KJ/mol | |
| C. | 浓硫酸与氢氧化钠溶液反应生成1molH2O(I),放出热量也等于57.3KJ | |
| D. | 稀CH3COOH溶液与稀NaOH溶液反应生成1molH2O(l),放出热量小于57.3KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
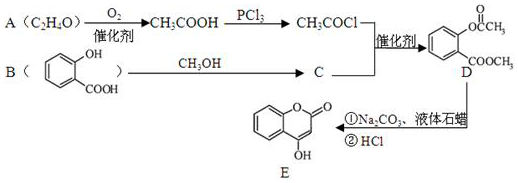
 .
.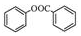 )的合成路线(无机原料任选).
)的合成路线(无机原料任选). .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 催化剂能使不起反应的物质发生反应 | |
| B. | 催化剂在化学反应前后,化学性质和质量都不变 | |
| C. | 催化剂能改变化学反应速率 | |
| D. | 任何化学反应,都需要催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在任何条件下,化学平衡常数都是一个定值 | |
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 | |
| C. | 化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 | |
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,22.4L水所含分子数目为NA | |
| B. | 1mol•L-1 K2SO4溶液所含K+数目为2NA | |
| C. | 1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA | |
| D. | O2的摩尔体积约为22.4 L•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收546.6 kJ热量 | |
| B. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于546.6 kJ | |
| C. | 相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量 | |
| D. | 2 mol H-F键的键能比1 mol H-H键和1 mol F-F 键的键能之和大546.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向煮沸的 1 mol•L-1 NaOH 溶液中滴加 FeCl3饱和溶液制备 Fe(OH)3 胶体 | |
| B. | 向混有醋酸的乙酸乙酯中加入饱和 Na2CO3溶液,振荡,分液分离除去乙酸乙酯中的少量醋酸 | |
| C. | 检验甲酸中是否含有甲酸丙酯时,可以往混合液中加入足量 NaOH 溶液以中和甲酸,再滴加银 氨溶液看是否产生银镜 | |
| D. | 用酸性高锰酸钾溶液除去乙烷中少量的乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、CH3COO-、Cl- | B. | Mg2+、Ba2+、Br- | ||
| C. | Mg2+、Cl-、I- | D. | Na+、NH4+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com