
| I1/KJ•mol-1 | I2/KJ•mol-1 | I3/KJ•mol-1 | I4/KJ•mol-1 | I5/KJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
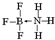 .
.
分析 (1)①Ti是22号元素其原子核外有22个电子,Ti原子失去两个电子生成Ti2+,该离子核外有1s、2s、2p、3s、3p、3d电子,电子占据的最高能级是3d能级,该能级具有的原子轨道数为5;
②BH4-中B原子价层电子对个数是4且不含孤对电子对,根据价层电子对互斥理论判断B原子的杂化方式;
(2)①电子层结构相同的离子,离子半径随着原子序数增大而减小;
②根据表中数据知,M原子核外有2个电子,位于第IIA族,在化合物中呈现+2价,H为-1价,根据化合价判断化学键;
(3)①结构相似的氢化物,含有氢键的物质熔沸点较高;
②NH3容易和分子中有空轨道的BF3反应形成新的化合物,N原子和B原子之间存在配位键;
(4)①非极性分子的溶质极易溶于非极性分子的溶剂;
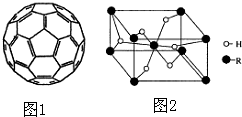
②根据图知,每个C原子含有σ 键个数=$\frac{1}{2}×3$=1.5;
(5)该晶胞中H原子个数=2+4×$\frac{1}{2}$=4,R原子个数=1+8×$\frac{1}{8}$=2,H、R原子个数之比=4:2=2:1;该晶胞体积=$\frac{\frac{M+2}{{N}_{A}}×2}{ρ}$.
解答 解:(1)①Ti是22号元素其原子核外有22个电子,Ti原子失去两个电子生成Ti2+,所以基态Ti2+中含有的电子数为20;该离子核外有1s、2s、2p、3s、3p、3d电子,电子占据的最高能级是3d能级,该能级具有的原子轨道数为5;
故答案为:20;3d;5;
②BH4-中B原子价层电子对个数是4且不含孤对电子对,根据价层电子对互斥理论知B原子的杂化方式为sp3,
故答案为:sp3;
(2)①电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径:Li+<H-,
故答案为:<;
②根据表中数据知,M原子核外有2个电子,位于第IIA族,在化合物中呈现+2价,为Mg元素,H为-1价,该化合物化学键为MgH2,
故答案为:MgH2;
(3)①结构相似的氢化物,含有氢键的物质熔沸点较高,氨气分子和膦分子结构相似,但氨气中含有氢键,导致熔沸点升高,
故答案为:氨气分子之间可以形成氢键;
②NH3容易和分子中有空轨道的BF3反应形成新的化合物,N原子和B原子之间存在配位键,其结构式为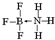 ,
,
故答案为: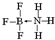 ;
;
(4)①非极性分子的溶质极易溶于非极性分子的溶剂,C60晶体易溶于苯、CS2,C60是非极性分子,故答案为:非极性;
②根据图知,每个C原子含有σ 键个数=$\frac{1}{2}×3$=1.5,1mol该物质中σ 键个数=1.5×60×1mol×NA/mol=90NA,故答案为:90NA;
(5)该晶胞中H原子个数=2+4×$\frac{1}{2}$=4,R原子个数=1+8×$\frac{1}{8}$=2,H、R原子个数之比=4:2=2:1,所以其化学式为H2R,该晶胞体积=$\frac{\frac{M+2}{{N}_{A}}×2}{ρ}$cm3=$\frac{2M+4}{a{N}_{A}}$cm3,
故答案为:H2R;$\frac{2M+4}{a{N}_{A}}$.
点评 本题考查物质结构和性质,涉及晶胞计算、相似相溶原理、氢键、原子核外电子排布等知识点,这些都是高频考点,难点是晶胞计算、价层电子对互斥理论,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
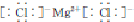 ,工业上用电解无水氯化镁而不是氧化镁获得镁的原因是消耗大量的电能.
,工业上用电解无水氯化镁而不是氧化镁获得镁的原因是消耗大量的电能.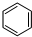 (g)+3H2(g) $?_{FeSO_{4}/Al_{2}O_{3}}^{高温}$
(g)+3H2(g) $?_{FeSO_{4}/Al_{2}O_{3}}^{高温}$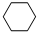 (g)
(g) 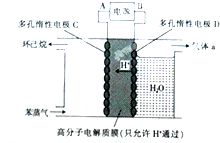
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠有还原性,可用作脱氧剂 | B. | FeCl3有氧化性,可用于制印刷电路 | ||
| C. | 铝有还原性,可冶炼某些金属 | D. | 浓硫酸有吸水性,可用于干燥氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
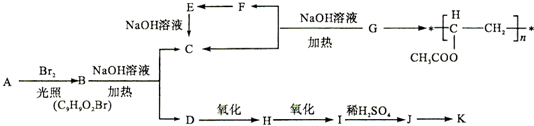
 .
.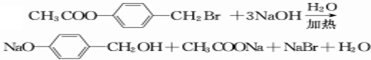 .
.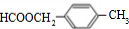 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸具有吸水性,能干燥氢气,也能干燥氨气 | |
| B. | 乙醛具有还原性,能被新制氢氧化铜浊液氧化,也能被溴水氧化 | |
| C. | SO2具有漂白性,能使品红褪色,也能使酸性KMnO4溶液褪色 | |
| D. | 硝酸属于强酸,能与CaCO3反应生成CO2气体,也能与CaSO3生成SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | 电离常数 |
| HF | Ka=3.5×10-4 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| HClO | Ka=3.2×10-8 |
| A. | 同温同浓度下,溶液的pH值:NaF>NaClO>Na2CO3 | |
| B. | 结合H+的能力:ClO->CO32->F- | |
| C. | 碳酸钠溶液中加入少量氢氟酸的离子方程式:CO32-+2HF═2F-+H2O+CO2↑ | |
| D. | 次氯酸钠溶液中通入少量二氧化碳的离子方程式:ClO-+CO2+H2O═HCO3-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ZnC2水解生成乙烷(C2H6 ) | B. | Al4C3水解生成丙炔(C3H4) | ||
| C. | Mg2C3水解生成丙炔(C3H4) | D. | Li2C2水解生成乙烯(C2H4) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com