
【题目】官能团的转化在有机合成中极为常见,能够在碳链上引入羟基反应是( )
①取代反应②加成反应③消去反应④水解反应⑤还原反应⑥氧化反应⑦酯化反应⑧硝化反应
A.①②⑥⑦B.①②④⑤C.③⑥⑦⑧D.②③⑤⑥
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A. 反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B. 根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸或硝酸在下列用途或反应中各表现的性质是:
A.强酸性 B.易挥发性 C.吸水性 D.脱水性 E.强氧化性 F.不稳定性
(1)胆矾中加入浓硫酸,久置变为白色粉末__________;
(2)用铝槽车装运浓硫酸或浓硝酸___________;
(3)浓硝酸敞口放置会“发烟”___________,
(4)浓硝酸久置会变黄____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)
根据图示回答下列问题:
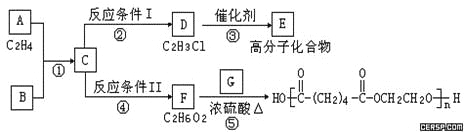
(1)写出A、E、G的结构简式:A ,E ,G ;
(2)反应②的化学方程式(包括反应条件)是 ,反应④化学方程式(包括反应条件)是 ;
(3)写出①、⑤的反应类型:① 、⑤ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物和人们生产生活密切相关
(1)某烃的密度为 3.21g/L(换算到标准状况下),充分燃烧 3.6g 该烃,生成 11g 二氧化碳和 5.4g 水。写 该烃的分子式为_______,并写出其可能存在的结构简式并用系统命名法命名____________________。
(2)某烃 A 是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平, A 还是一种植 物生长调节剂,A 可发生如图所示的一系列化学反应,③是实验室制取 A 的反应。根据左图写出相应的化学 方程式并注明反应类型。

②_________________, 反应类型_________________。
③_________________, 反应类型_________________。
④_________________, 反应类型_________________。
⑤_________________, 反应类型_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏加德罗常数)( )
A. 12 g石墨中含有C—C键的个数为1.5 NA
B. 12 g金刚石中含有C—C键的个数为4 NA
C. 60 g SiO2中含有Si—O键的个数为2 NA
D. 124 g P4中含有P—P键的个数为4 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。

实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
(1)配制混酸的方法是_______________________。反应中需不断搅拌,目的是__________________________________________。
(2)仪器A的名称是______,使用该仪器前必须进行的操作是____。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_____。
(4)分离反应后产物的方案如下:

其中,操作1的名称为______,操作2中需要使用下列仪器中的____(填序号)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(5)该实验中一硝基甲苯的产率为______(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来AIST报告正在研制一种“高容量、低成本”锂-铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )

A. 放电时,Li+透过固体电解质向Cu极移动
B. 放电时,负极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH-
C. 通空气时,铜被腐蚀,表面产生Cu2O
D. 整个反应过程中,铜相当于催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁—次氯酸盐燃料电池的工作原理如右图所示,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-

下列有关说法正确的是( )
A.电池工作时,c溶液中的溶质一定是MgCl2
B.负极反应式:ClO--2e-+H2O=Cl-+2OH-
C.电池工作时,OH-向b电极移动
D.b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com