
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϡ���ҵ�����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�������������Ӧ���£�
��CO(g)+2H2(g) ![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g) ![]() CH3OH��g��+H2O(g) ��H����58 kJ/mol
CH3OH��g��+H2O(g) ��H����58 kJ/mol
��CO2(g)+H2(g) ![]() CO(g)+H2O(g) ��H����41 kJ/mol
CO(g)+H2O(g) ��H����41 kJ/mol
�ش��������⣺
��1����֪��Ӧ������صĻ�ѧ�������������£�
��ѧ�� | H��H | C��O | C | H��O | C��H |
E/��kJ��mol-1�� | 436 | 343 | 1076 | 465 | x |
��x����
��2������lmol CO2��2mol H2�����ݻ�Ϊ2L�ĺ����ܱ������У������ֲ�ͬ�¶��·�����Ӧ�ڡ����CH3OH�����ʵ�����ʱ��ı仯��ͼ��ʾ��
������I�����Ӧ��ƽ�ⳣ����С��ϵΪKIK��(�������������)��
��һ���¶��£����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬������
a��������ѹǿ���� b���״���ˮ����������ȱ��ֲ���
c��v����H2����3v����CH3OH�� d��2��C��O���ѵ�ͬʱ��6��H��H����
����5min��Ӧ�ﵽƽ��״̬��H2��ת����Ϊ90%������CO2��ʾ��ƽ����Ӧ����Ϊ �� ���¶��µ�ƽ�ⳣ��Ϊ���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ�����
a����С��Ӧ�������ݻ� b��ʹ�ú��ʵĴ���
c������He d����ԭ�����ٳ���CO2��H2
��3���Լ״�Ϊȼ�ϣ�����Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ�ء��Դ˵������Դ����ʵ������ģ������Ʒ���桰�ۻ����������̣�װ����ͼ��ʾ������������b�� �� �����缫��ӦΪ��
���𰸡�
��1��413
��2������ac��0.06mol/��L��min����450��ad
��3���״���CH3OH����2Al-6e- +3H2O=A12O3+6H+
���������⣺��1����֪��
��CO(g)+2H2(g) ![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g) ![]() CH3OH��g��+H2O(g) ��H����58 kJ/mol
CH3OH��g��+H2O(g) ��H����58 kJ/mol
��CO2(g)+H2(g) ![]() CO(g)+H2O(g) ��H����41 kJ/mol
CO(g)+H2O(g) ��H����41 kJ/mol
���ݸ�˹���ɿ�֪��һ�ۼ��õ���Ӧ�ٵġ�H1=-99 kJ/mol�����ݱ��м��ܿ�֪1076+2��436-3x-343-465=-99�����x=413����2�������ߢ����ȴﵽƽ��״̬��˵�����ߢ���¶ȸ������ߢ���������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ������У�ƽ�ⳣ����С�����Զ�Ӧ��ƽ�ⳣ����С��ϵΪK��>K��;��a.����Ӧ�����С����������ѹǿ����˵���ﵽƽ��״̬��a��ȷ��b���ݷ���ʽ��֪�״���ˮ�����������ʼ����1:1������˵���ﵽƽ��״̬��b����v����H2����3v����CH3OH����ʾ���淴Ӧ������ȣ��ﵽƽ��״̬��c��ȷ��d.���ݷ���ʽ��֪2��C=O���ѵ�ͬʱһ����6��H-H���ѣ�����˵���ﵽƽ��״̬��d����ѡac��
��
CO2��g��+ | 3H2��g�� | CH3OH��g��+ | H2O��g�� | |
��ʼŨ�ȣ�mol/L�� | 0.5 | 1 | 0 | 0 |
�仯Ũ�ȣ�mol/L�� | 0.3 | 0.9 | 0.3 | 0.3 |
ƽ��Ũ�ȣ�0mol/L�� | 0.2 | 0.1 | 0.3 | 0.3 |
����CO2��ʾ��ƽ����Ӧ����Ϊ:0.3mol/L��5min=0.06mol/��L��min��;���¶��µ�ƽ�ⳣ��Ϊ0.3��0.3/0.2��0.13=450
a.����Ӧ�����С����С��Ӧ�������ݻ�ƽ��������Ӧ������У��״��IJ������ߣ�a��ȷ��
b.ʹ�ú��ʵĴ���ƽ�ⲻ�ƶ������ʲ��䣬b����c�����ݻ����䣬����He,������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ����Բ�����Ӱ�죬c����;d.��ԭ�����ٳ���CO2��H2�൱������ѹǿ��ƽ��������Ӧ������У��״��IJ������ߣ�d��ȷ;��ѡa����3��ģ������Ʒ���桰�ۻ�����������缫�������������Դ����������������a������������b�����Ǽ״�����Ϊ�������ᷢ��������Ӧ�������γ�����Ĥ��������ˮ�μӣ����Ե缫��ӦʽΪ2Al-6e- +3H2O=A12O3+6H+
�����㾫����������Ĺؼ��������ⷴӦ�Ⱥ��ʱ�����֪ʶ�������ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȣ��Լ��Ի�ѧƽ��״̬���ʼ����������⣬�˽⻯ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������SO2��������Ҫ�Ŀ�������ָ�꣮
��1��ij����SO2���ŷ����涨���ó���0.10mg/��L�̵�������Ϊ�ⶨ�ù����ŷŵ��̵�����SO2�ĺ�����ijͬѧij�γ�ȡ��30.00L�̵�������ͨ��1Lˮ����SO2��ȫ�����գ�����Һ���Ϊ1L����1.0��10��3mol/L�ı��͵�ˮ���ܶ�Ϊ1g/cm3���ζ�����ӦΪSO2+I2+2H2O�TH2SO4+2HI��ʵ������¼�������£�
����SO2����Һ��� | ���͵�ˮ��� | ָʾ�� | |
��һ�� | 25.00mL | 6.05 | 2��3�ε��� |
�ڶ��� | 25.00mL | 7.20 | 2��3�ε��� |
������ | 25.00mL | 5.95 | 2��3��� |
a.ȡ25.00ml���̵�����ˮ��Һ��������������
b.�ζ��յ��־Ϊ
c.�ó��ŷŵ��̵�����SO2�ĺ���Ϊmg/��L�̵�����
��2����ͬѧ��ʵ���һ���֤��SO2�ܷ���BaCl2��Һ��Ӧ��ʵ�飮��������ͨ���Ȼ�����Һ�������ϲ�������������������SO2ͨ��װ��1mol/LBaCl2��Һ���Թ��к����˰�ɫ�����
a.�ð�ɫ������Ϊ �� �����������ԭ�������
b.Ϊ�˱��������������ͬѧ���������ʵ��װ�ã�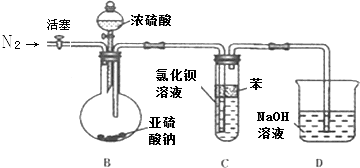
��ش���������
�ٷ�Ӧ��ʼǰ��������ȡSO2��װ����ͨ�봿����N2 �� �������ǣ� ��
�ڸ�ͬѧ��ΪBa��NO3��2��Һ��BaCl2��Һһ������������SO2Ҳ���ᷴӦ�������ж����������ȷ�������������粻��ȷ��д��SO2��Ba��NO3��2��Һ��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʹFeSO4��KSCN�����Һ��Ϊ��ɫ���Լ���
A. ϡ���� B. ������ˮ C. ��������Һ D. ����ʯ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(SO2Cl2)��һ����Ҫ�Ļ����Լ���ʵ���Һϳ������ȵ�ʵ��װ������ͼ��ʾ��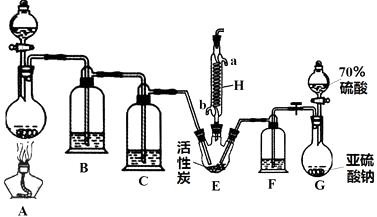
��֪���� SO2(g)+Cl2(g) ![]() SO2Cl2(l) ��H����97kJ/mol��
SO2Cl2(l) ��H����97kJ/mol��
�� �����ȳ�����Ϊ��ɫҺ�壬�۵�Ϊ-54.1�棬�е�Ϊ69.1�棬�ڳ�ʪ�����С����̡���
�� 100�����ϻ�ʱ���������ȶ��ֽ⣬���ɶ��������������
�ش��������⣺
��1���������ڳ�ʪ�����С����̡���ԭ�������û�ѧ����ʽ��ʾ����
��2������װ��G�����Եķ�������
��3��װ��A�з�����Ӧ�����ӷ���ʽΪ��
��4��H�������� �� ����ˮ���ķ�����������a��b����
��5��װ��C��F�е��Լ���ͬ��ʢ�ŵ��Լ�Ϊ��
��6����װ�ô��ڵ�һ��ȱ������
��7������SO2��Cl2����һ������ͨ��ˮ�У�����Ƽ�ʵ����֤�����Ƿ�ǡ����ȫ��Ӧ(��Ҫ����ʵ�鲽�衢����ͽ���)��
��������ѡ����ѡ���Լ����μӷ�̪������������Һ���Ȼ�������Һ�����軯����Һ��Ʒ����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaOH��KOH�ȼ�����Һ�������������������Լ�ƿ��
A. ���в�������ϸ��ƿ B. ���в������Ĺ��ƿ
C. ���ιܵĵ�ƿ D. ����������ϸ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����Ĺ�ҵ��ˮ�к��д�����FeSO4 �� �϶��CuSO4������Na2SO4 �� Ϊ�˼�����Ⱦ�����Ϊ���������ƻ��Ӹ÷�ˮ�л������������ͽ���ͭ���������������ͼ����ɻ�������������ͭ��ʵ�鷽�������ɹ�ѡ����Լ�Ϊ���ۡ�ϡH2SO4��NaOH��Һ���Լ��� 
��1������a������Ϊ �� ����Ҫ�IJ�������Ϊ ��
��2������E�ijɷ�Ϊ �� ������Լ���Ϊ �� �����Ļ�ѧ����ʽΪ ��
��3�������Լ��ٵ�Ŀ���� ��
��4������ҺD����ҺG�еõ�FeSO4.7H2O����IJ���Ϊ����ȴ�ᾧ����ϴ�ӡ����
��5������ˮ����������������ͭ����������ɵĻ����Һ������c��Cu2+��=0.1mol/L��c��Fe2+��=0.4mol/L��c��SO ![]() ��=0.6mol/L����֪������Ũ�Ⱥ��Բ��ƣ���c��Na+��Ϊ ��
��=0.6mol/L����֪������Ũ�Ⱥ��Բ��ƣ���c��Na+��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.�������Ƶ�Ħ��������40g
B.�����ʵ���Ũ�����ɼ��Ϊ����Ũ����
C.�����ӵ������ĵ�λ��mol-1
D.1 mol�κ�������ռ�������22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ������Ϣ���ó��Ľ�����ȷ���ǣ� �� 
A.̼��ȼ����Ϊb kJ/mol
B.2C��s��+O2��g���T2CO��g����H=��2��b��a�� kJ/mol
C.2CO2��s���T2CO��g��+O2��g����H=+a kJ/mol
D.C��s��+O2��g���TCO2��g����H����b kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʣ�CH3COOH��NaOH��NH3H2O��CH3COONa��NaCl����������������ʵ��� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com