
| A. | 检验某有机物中是否含有醛基:取少量水溶液于试管中,加入过量氢氧化钠溶液和新制Cu(OH)2悬浊液,加热至沸腾,看是否有砖红色沉淀生成 | |
| B. | 提纯混有少量CaCl2的NaCl固体:将固体配成溶液,加入稍过量Na2CO3溶液至沉淀完全,过滤,再向滤液中加入稍过量盐酸,蒸发结晶 | |
| C. | 验证某无色溶液中存在SO42-:向试管中加入少量待测溶液,然后加入少量BaCl2溶液,后加入足量稀硝酸,观察到最后仍有白色沉淀生成即可 | |
| D. | 验证炭与浓硫酸反应产生的CO2:将炭与浓硫酸反应生成的气体通入盛有澄清石灰水的试管中,观察是否有白色沉淀生成 |
分析 A.在保证溶液呈碱性的条件下可直接加入新制Cu(OH)2悬浊液;
B.氯化钙和碳酸钠反应生成碳酸钙沉淀,过滤后加入盐酸可除去碳酸钠;
C.加入少量BaCl2溶液,可生成AgCl沉淀;
D.炭与浓硫酸反应生成二氧化硫,也可与澄清石灰水反应生成沉淀.
解答 解:A.在保证溶液呈碱性的条件下可直接加入新制Cu(OH)2悬浊液,无需加入氢氧化钠溶液,故A错误;
B.氯化钙和碳酸钠反应生成碳酸钙沉淀,过滤后加入盐酸可除去碳酸钠,蒸发结晶可得到氯化钠,故B正确;
C.加入少量BaCl2溶液,可生成AgCl沉淀,应先加入盐酸,如无现象再加入氯化钡溶液检验,故C错误;
D.炭与浓硫酸反应生成二氧化硫,也可与澄清石灰水反应生成沉淀,应将反应后的气体先通过高锰酸钾除去二氧化硫,用品红检验是否完全除去,然后再用澄清石灰水检验,故D错误.
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及物质的检验、分离提纯等,把握反应原理及反应与现象的关系为解答的关键,注意从实验的评价性及物质性质分析解答,题目难度不大.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.2 mol•L-1硫酸铁溶液中含有的SO42-数为0.6NA | |
| B. | 60 g SiO2晶体中含有2NA个Si-O键 | |
| C. | 1L浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,水浴加热 | |
| B. | 测量溶液的导电性 | |
| C. | 向两种溶液中分别滴加硝酸银溶液 | |
| D. | 尝味道 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
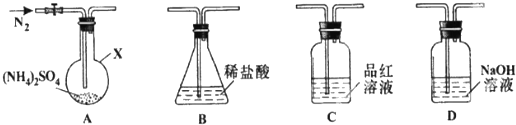
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氯是纯净物,而氯水是混合物 | B. | 液氯有酸性,氯水有漂白性 | ||
| C. | 液氯较氯水的漂白作用更强 | D. | 液氯无色,氯水呈黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH3可以用来做喷泉实验是因为其有特殊气味 | |
| B. | 工业上用氨和二氧化碳合成尿素属于氮的固定 | |
| C. | 液氨作制冷剂原因是其气化时大量吸收周围的热量 | |
| D. | NH3能使无色酚酞溶液变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
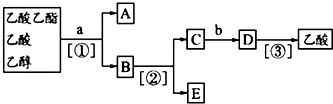
| A. | ①蒸馏 ②过滤 ③分液 | B. | ①分液 ②蒸馏 ③蒸馏 | ||
| C. | ①蒸馏 ②分液 ③分液 | D. | ①分液 ②蒸馏 ③结晶 过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
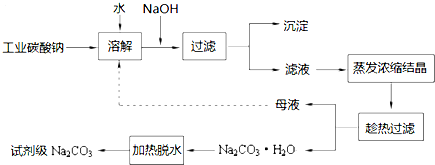
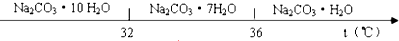
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com